 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列混合溶液属于缓冲溶液的有()
B.NaHCO3和Na2CO3
C.过量的氨水和HCI
D.等物质量H3P04和Na2HPO4
E.HCI和NaCl
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
B.NaHCO3和Na2CO3
C.过量的氨水和HCI
D.等物质量H3P04和Na2HPO4
E.HCI和NaCl
 更多“下列混合溶液属于缓冲溶液的有()”相关的问题
更多“下列混合溶液属于缓冲溶液的有()”相关的问题
A.50m10.2mol/L-1CHlCOOH和50ml0.1moI/L-1NaOH混合
B.50m10.1mol/L-1CH3COOH和50ml0.1mol/L-1NaOH混合
C.50m10.1mol/L-1CH3COOH和50ml0.2mol/L-1NaOH混合
D.50m10.2mol/L-1HCI和50ml0.1mol/L-1NH3H20混合
A. 50mL0.2mol/LCH3COOH和50mL0.1mol/LNaOH混合
B. 50mL0.1mol/LCH3COOH和50mL0.1mol/LNaOH混合
C. 50mL0.1mol/LCH3COOH和50mL0.2mol/LNaOH混合
D. 50mL0.2mol/LHCl和50mL0.1mol/LNH3H2O混合
A、0.10 mol·L-1 NH3--1.00mol·L-1 NH4Cl;
B、1.00mol·L-1 NH3--0.10mol·L-1 NH4Cl;
C、1.00mol·L-1 NH3--1.00 mol·L-1NH4Cl;
D、0.10 mol·L-1 NH3--0.10 mol·L-1 NH4Cl
(1)拟将下列离子转化为碳酸正盐,试说明怎样选择沉淀剂,并写出反应方程式:
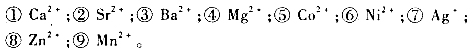
(2)从二氧化硅氯化制备SiCl4,需要和焦炭共热进行反应的耦合:
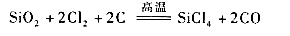
而用HF对二氧化硅进行氟化制备SiF4则不需要反应的耦合:

(3)Pb与稀盐酸反应,速率很慢且反应会停止;但与浓盐酸作用时,反应容易进行。试给出合理解释。
(4)从H3BO3显酸性的机理去说明为什么H3BO3是一元弱酸。
(5)试解释下列无机含氧酸的氧化性由强到弱的原因:
HClO4>H2SO4>H3PO4>H2SiO3
(6)为什么硅不与氧化性酸反应,但又可溶于HNO3及HF混合溶液中?
(7)用平面图示的方法表示单聚硅酸根SiO44-,焦硅酸根Si2O74-,链三聚硅酸根和环六聚硅酸根。写出链n聚和环n聚多硅酸根的化学式。
(8)画简图表示乙硼烷的结构,并说明其中3中心2电子键的形成过程。
(9)硼砂Na2[B4O5(OH)4]·8H2O是四硼酸的钠盐。试说明通常将硼砂的化学式写成Na2B4O7原因。为什么硼砂溶于水形成缓冲溶液?试计算其pH。
(10)三氟化硼分子是单聚体BF3,同样属于缺电子结构的乙硼烷分子却是B2H6。或者说是二聚的BH3。从结构角度如何解释这种现象?
(11)BiI5和PbI4均不能稳定存在,却有TU3存在,试说明其原因。
(12)试比较乙硼烷、烷烃、甲硅烷三者的热稳定性,写出其受热分解的化学反应方程式。
A、氨水中加入过量 HCl 的混合溶液
B、NaCl加入适量 HCl 的混合溶液
C、NaH2PO4与 Na2HPO4的混合溶液
D、0.1 mol·dm-3 HAc 与 0.1 mol·dm-3 NaOH


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题