 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
今有三种酸(CH3)2AsO2H,ClCH2COOH,CH3COOH,它们的标准解离常数分别为6.4×10-7,1.4×10-3,1.8×10-5。试问:
(1)欲配制pH=6.50缓冲溶液,用哪种酸最好?
(2)需要多少克这种酸和多少克NaOH以配制1.00L缓冲溶液,其中酸和它的共轭碱的总浓度等于1.00mol·L-1?
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 更多“有三种酸,CH2ClCOOH、HCOOH 和CH3COOH,…”相关的问题
更多“有三种酸,CH2ClCOOH、HCOOH 和CH3COOH,…”相关的问题
今有三种酸(CH3)2AsO2H,ClCH2COOH,CH3COOH,它们的标准解离常数分别为6.4×10-7,1.4×10-3,1.8×10-5。试问:
(1)欲配制pH=6.50缓冲溶液,用哪种酸最好?
(2)需要多少克这种酸和多少克NaOH以配制1.00L缓冲溶液,其中酸和它的共轭碱的总浓度等于1.00mol·L-1?
有三种酸(CH3)2AsO2H,ClCH2COOH,CH3COOH.它们的标准解离常数分别是6.4×10-7,1.4×10-5,1.76×10-5。试问(1)欲配制pH=6.50的缓冲溶液,用哪种酸最好?(2)配制1.00L这种缓冲溶液(其中酸和它的对应盐的总浓度等于1.00mol·L-1)需要多少克这种酸和多少克NaOH?
已知25℃时下列弱酸的解离常数:
HOC1 Ka=3.5×10-8、HAc Ka=1.8×10-5、H5PO4 Ka1=7.5×10-5,
问配制pH=4的缓冲溶液时,哪种酸最好?计算需要多少克这种酸和多少克NaOH才能配制成1L总浓度为1mol.L-1的缓冲溶液。
已知:pKayΘ(HCOOH)=3.75,pKayΘ(HAc)=4.75,p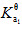 (H3PO4)=2.12;欲配制pH=3.5的缓冲溶液500mL,并使溶液中酸的浓度为0.20mol•L-1。应选用哪种缓冲对?需称取多少固体钠盐?
(H3PO4)=2.12;欲配制pH=3.5的缓冲溶液500mL,并使溶液中酸的浓度为0.20mol•L-1。应选用哪种缓冲对?需称取多少固体钠盐?
欲配制pH=9.00的缓冲溶液,最好应选用()。
A.NaHCO3一Na2CO3
B.NaH2PO4一Na2HPO4
C.HOAc—NaOAc
D.NH3.H2O—NH4Cl
A.NH2OH(羟氨)(pKb=8.04)
B. NH3·H2O(pKb=4.74)
C. CH3COOH(pKa=4.74)
D. HCOOH(pKa=3.74)
A.NH2OH(羟氨)(pKb=8.04)
B.NH3·H2O(pKb=4.74)
C.CH3COOH(pKa=4.74)
D.HCOOH(pKa=3.74)
A.NaH2PO4-Na2HPO4(pK(H2PO4-)=7.21)
B.HAc-NaAc(pK(HAc)=4.76)
C.HCOOH-HCOONa(pK(HCOOH)=3.75)
D.NH3-NH4Cl (pK(NH3)=4.75)


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题