 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
4g NaOH固体溶解后配制成100mL 溶液,其物质的量浓度为 mol/L ,取出10mL 该溶液,它的物质的量浓度为 mol/L,将取出的10mL加水稀释至100mL, 其物质的量浓度为 mol/L。(已知:NaCl的摩尔质量为40g/mol)
提问人:网友shifor1983
发布时间:2022-01-07
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 更多“4g NaOH固体溶解后配制成100mL 溶液,其物质的量浓…”相关的问题
更多“4g NaOH固体溶解后配制成100mL 溶液,其物质的量浓…”相关的问题
A、0.1 mol/L HCl 溶液
B、0.1 mol/L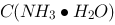 溶液
溶液
C、0.1 mol/L HAc溶液
D、0.1 mol/L HAc溶液 +0.1 mol/L NaAc溶液
微溶化合物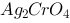 在0.0010 mol/L的
在0.0010 mol/L的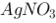 溶液中的溶解度比在0.0010 mol/L的
溶液中的溶解度比在0.0010 mol/L的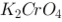 溶液中的溶解度
溶液中的溶解度
A、大
B、小
C、相等
D、大一倍
室温下,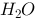 水的电离达到平衡,下列叙述正确的是:
水的电离达到平衡,下列叙述正确的是:
A、将水加热,平衡正向移动,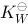 变小
变小
B、向水中加入NaOH固体,平衡逆向移动,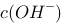 增大
增大
C、新制氯水久置后,水的电离平衡正向移动,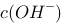 增大
增大
D、向水中加入少量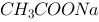 固体,平衡正向移动,
固体,平衡正向移动,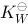 增大
增大
在含有同浓度的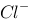 和
和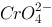 的混合溶液中,逐滴加入
的混合溶液中,逐滴加入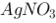 溶液,发生的现象是:
溶液,发生的现象是:
A、AgCl先沉淀
B、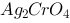 先沉淀
先沉淀
C、AgCl和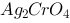 同时沉淀
同时沉淀
D、以上都错
A、缓冲溶液一般由较大浓度的弱酸及其共轭碱组成;
B、缓冲溶液有抗碱,抗酸和抗稀释的作用;
C、.缓冲溶液是同离子效应的应用;
D、缓冲溶液的缓冲能力是无限的;


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题