 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
306K时,反应N2O4(g)=2NO2(g)的=0.26.在容积为10L的容器中加入4.0molN2O4
306K时,反应N2O4(g)=2NO2(g)的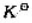 =0.26.在容积为10L的容器中加入4.0molN2O4和1.0molNO2,则开始时p(总)=()kPa,反应向()方向进行。
=0.26.在容积为10L的容器中加入4.0molN2O4和1.0molNO2,则开始时p(总)=()kPa,反应向()方向进行。
提问人:网友yaoshiyu
发布时间:2022-01-07
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
306K时,反应N2O4(g)=2NO2(g)的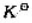 =0.26.在容积为10L的容器中加入4.0molN2O4和1.0molNO2,则开始时p(总)=()kPa,反应向()方向进行。
=0.26.在容积为10L的容器中加入4.0molN2O4和1.0molNO2,则开始时p(总)=()kPa,反应向()方向进行。
 更多“306K时,反应N2O4(g)=2NO2(g)的=0.26.…”相关的问题
更多“306K时,反应N2O4(g)=2NO2(g)的=0.26.…”相关的问题
A、两个反应的∆rGmΘ相等
B、两个反应的∆rHmΘ相等
C、对两个反应而言,ξ=1 mol时表示都消耗了1 mol的NO2
D、ξ=1 mol时表示第一个反应增加了1 mol N2O4,第二个反应减少了1 mol的NO2
反应:2N2O5(g)====4NO2(g)+O2(g)
起始时N2O5(g)浓度为1.15mol·dm-3,100s后测得N2O5(g)浓度为1.0mol·dm-3,则反应在100s内的平均速率为多少?
A. (2)自发(1)不自发
B. (1)和(2)都不自发
C. (1)自发(2)不自发
D. (1)和(2)都自发
A、1800
B、90000
C、6000
D、798
A、(Kp,1Ɵ)2=K p,2Ɵ
B、Kp,1Ɵ=K p,2Ɵ
C、Kp,1Ɵ=(K p,2Ɵ)2
D、Kp,1Ɵ=1/K p,2Ɵ


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题