 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
利用以下298K时的数据计算298K时HCI(g)的摩尔生成焓:
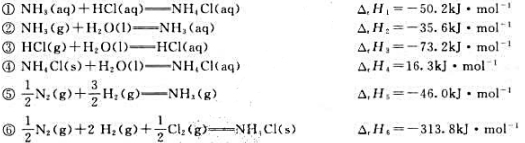
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 更多“利用以下298K时的数据计算298K时HCI(g)的摩尔生成…”相关的问题
更多“利用以下298K时的数据计算298K时HCI(g)的摩尔生成…”相关的问题
试利用标准电极电势的数据(表5.5)计算298K时反应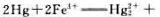
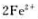 的平衡常数
的平衡常数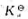 .
.
查表列出298K时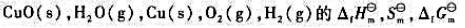 等热力学数据,试据此计算下列反应298K时的
等热力学数据,试据此计算下列反应298K时的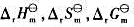 和1000K时的
和1000K时的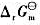 ,并进一步讨论反应的逆转温度。
,并进一步讨论反应的逆转温度。
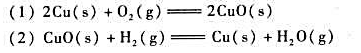
已知下列100kPa,298K时的热力学数据:
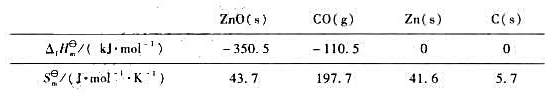
(1)试通过热力学计算,说明下面反应298K时的进行方向:
ZnO(s)+C(s)=Zn(s)+CO(g)
(2)求算上面反应自发正向进行的最低温度。
计算298K时,0.05mol·L-1HAc和0.05mol·L-1HCN的解离度各为多少?
计算下列等温反应(298K)的△rGmΘ: C6H6(g)+C2H2(g)→C6H5C2H3(g) 已知298K时C6H5C2H3的△fHmΘ=147.36J/(K.mol),SmΘ=345.1J/(K.mol)。
已知反应在298K的热力学数据如下:CO2(g)+H2=====CO(g)+H2O(g)
2010040 已知反应在298K的热力学数据如下:
CO2(g)+H2=====CO(g)+H2O(g)
ΔfH (kJ·mol-1) -393.5 0 -110.5 -241.8
求:
(1)298K时的反应的焓变;
(2)若此系统在400K时各组分气体的分压为p(CO)=p(H2O)=125kPa,p(CO2)=p(H2)=25kPa,通过计算判断反应进行的方向.已知298K时的平衡常数K=1.25


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题