 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
某温度下,反应的Kc=8.10×103,试求H2()的起始浓度分别为10.00mol·dm -3 和1.00mol·dm -3 时,Br 2 的转化率
提问人:网友hejun_7777
发布时间:2022-01-07
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 更多“某温度下,反应的Kc=8.10×103,试求H2()的起始浓…”相关的问题
更多“某温度下,反应的Kc=8.10×103,试求H2()的起始浓…”相关的问题

的Kc=8.10×103,试求H2(g)和Br2(g)的起始浓度均为1.00mol·dm-3时和H2(g)和Br2(g)的起始浓度分别为10.00mol·dm-3和1.00mol·dm-3时,Br2的平衡转化率。
可逆反应CO+H2O CO2+H2在密闭容器中建立平衡,在749K时该反应的平衡常数Kc=2.6。
(1)当CO 起始浓度为2mol/L,H2O 起始浓度为2mol/L 时,CO 的转化率为多少?
(2)当CO 起始浓度仍为2mol/L,H2O 的起始浓度为6mol/L 时,CO 的转化率为多少?
(3)从计算结果说明浓度对化学平衡移动的影响。
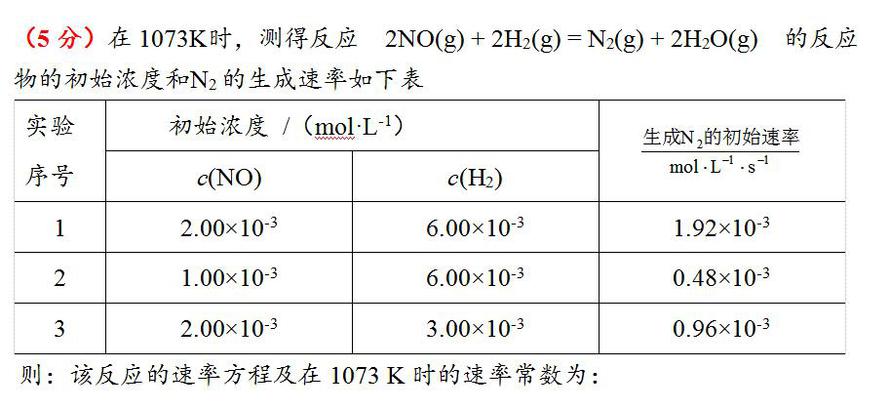
A、v = kc2(NO)c(H2)
B、k = 8.00×104 L2·mol-2·s-1
C、v = kc(NO)c2(H2)
D、v = kc2(NO)c2(H2)
E、不能确定
A、反应将向生成更多的HBr方向进行
B、反应向消耗H2的方向进行
C、反应已经达到平衡
D、反应向生成更多Br2 的方向进行
B.2
C.3
D.4


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题