 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列体系电位滴定至化学计量点时的电池电动势(用SCE作负极)为多少?(a)在1mol·L-1HCL介
下列体系电位滴定至化学计量点时的电池电动势(用SCE作负极)为多少?
(a)在1mol·L-1HCL介质中,用Ce4+滴定Sn2+;
(b)在1mol·L-1H2SO4介质中,用Fe3+滴定UIV;
(c)在lmol·L-1H2SO4介质中,用Ce4+滴定vo2+.
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列体系电位滴定至化学计量点时的电池电动势(用SCE作负极)为多少?
(a)在1mol·L-1HCL介质中,用Ce4+滴定Sn2+;
(b)在1mol·L-1H2SO4介质中,用Fe3+滴定UIV;
(c)在lmol·L-1H2SO4介质中,用Ce4+滴定vo2+.
 更多“下列体系电位滴定至化学计量点时的电池电动势(用SCE作负极)…”相关的问题
更多“下列体系电位滴定至化学计量点时的电池电动势(用SCE作负极)…”相关的问题
(-)Pt,H2(1atm)|HA‖SCE()
以0.1000 mol/LNaOH溶液滴定弱酸HA溶液。当酸HA被中和一半时,电池电动势为0.504V;化学计量点时,电池电动势为0.729V。
计算: ①弱酸HA的Ka?
②原弱酸HA的浓度?(φSCE=0.242V)
准确量取30.00 mL弱酸HA,加水稀释至100.00 mL,在电池:(—)SHE|HA || SCE()中,以0.100 0 mol·L-1NaOH标准溶液滴定之。25℃时,当弱酸HA被中和一半时,电池电动势为0.524 V,化学计量点时,电池电动势为0.749 V。求:(1)弱酸HA的电离常数Kα值。(2)原弱酸HA溶液的浓度?(已知饱和甘汞电极的电极电位为0.244 V)
在1mol/L H2SO4介质中用Ce4+滴定Fe2+,滴定突跃范围是______,化学计量点时的电位φsp=______,二苯胺磺酸钠______(合适或不合适)作指示剂。
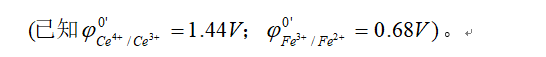
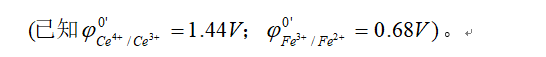
用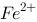 滴定
滴定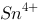 时,下列有关滴定曲线的叙述中不正确的是()
时,下列有关滴定曲线的叙述中不正确的是()
A、滴定百分率为25%处的电位为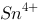 /
/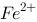 电对的条件电位
电对的条件电位
B、滴定百分率为50%处的电位为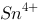 /
/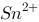 电对的条件电位
电对的条件电位
C、滴定百分率为100%处的电位为计量点电位
D、滴定百分率为200%处的电位为 /
/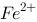 电对的条件电位
电对的条件电位
以0.01667mol/L K2Cr2O7标准溶液滴定0.1000mol/L的Fe2+至终点时,溶液的pH=2.0,求化学计量点电位。


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题