 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某温度下,反应的实验数据如下表所示: 则该反应的速率方程是()。A、 B、 C、 D、
某温度下,反应 的实验数据如下表所示:
的实验数据如下表所示:
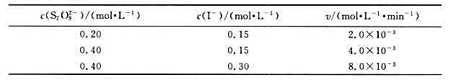
则该反应的速率方程是()。
A、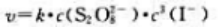
B、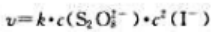
C、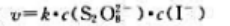
D、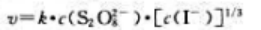
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某温度下,反应 的实验数据如下表所示:
的实验数据如下表所示:

则该反应的速率方程是()。
A、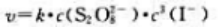
B、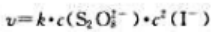
C、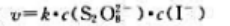
D、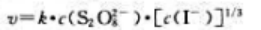
 更多“某温度下,反应的实验数据如下表所示: 则该反应的速率方程是(…”相关的问题
更多“某温度下,反应的实验数据如下表所示: 则该反应的速率方程是(…”相关的问题
进行氢氧化钠与乙酸乙酯的反应,实验数据如下表所示,求反应级数与反应速率常数。
时间t(s) | NaOH(mol/L) | CH3COOC2H5(mol/L) |
0 | 0.5638 | 0.3114 |
393 | 0.4866 | 0.2342 |
669 | 0.4467 | 0.1943 |
1010 | 0.4113 | 0.1589 |
1265 | 0.3879 | 0.1354 |
实验测得化学应A+2B-→3C在298.15K时的速率和浓度的关系如下表所示:
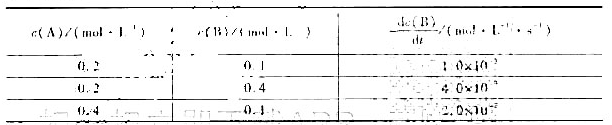 (1)写出反应的速率方程;
(1)写出反应的速率方程;
(2)求出反应级数:
(3)求反应的速率常数。
一定温度下,对反应2A====B+D,实验测定了如下数据:
cA/(mol·L-1) 0.40 0.20
速率/(mol·L-1·min-1) 0.02 0.01
则该反应的速率方程为r=______,速率常数k=______。
测量某导线在一定温度x下的电阻值y,如下表所示: 则利用一元线性回归方程,该导线电阻与温度之间拟合直线的斜率近似为()。
则利用一元线性回归方程,该导线电阻与温度之间拟合直线的斜率近似为()。
 , 且该反应的
, 且该反应的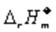 =-197.8kJ/mol。 欲使该反应在标准态时自发进行,则需要的温度条件是:
=-197.8kJ/mol。 欲使该反应在标准态时自发进行,则需要的温度条件是:
A.>1045K
B.=1045K
C.<1054k<br>
D.<1045k<br>
测量某导线在一定温度x下的电阻值y,如下表所示: 则利用一元线性回归方程,该导线电阻与温度之间拟合直线的斜率近似为()(4位有效数字)。
则利用一元线性回归方程,该导线电阻与温度之间拟合直线的斜率近似为()(4位有效数字)。
在一定条件下,反应H2(g)+Br2((g)→2HBr(g)的速率方程符合速率方程的一般形式,即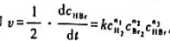 .
.
在某温度下,当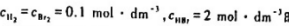 时,反应速率为v.其他不同浓度时的速率如下表所示:
时,反应速率为v.其他不同浓度时的速率如下表所示:

求反应的分级数n1、n2、n3.
某反应A→C+D的速率方程为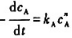 在300K下开始反应时只有A.实验过程中测得以下数据:
在300K下开始反应时只有A.实验过程中测得以下数据:

则此反应的级数为().
A.零级
B.一级
C.3/2级
D.二级
对于有机物与苯的反应,实验得到的数据如下表所示。
| 温度/℃ | 反应速度常数/(L·mol-1·h-1) |
| 0 20 40 60 80 100 | 5.20 12.0 21.0 39.0 60.0 83.0 |
(1)根据40℃~100℃的反应速度常数,确定阿累尼乌斯方程(教材式7-133)的常数
(2)根据以上结果,求75℃时的反应速度常数K,列出所有的假定条件。


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题