 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在酸性溶液中,Mn的元素电势图为:(1)计算;(2)Mn的哪几种氧化态在酸性条件下不稳定易歧化?
在酸性溶液中,Mn的元素电势图为:
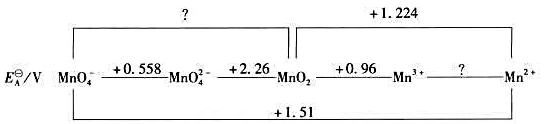
(1)计算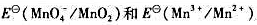 ;
;
(2)Mn的哪几种氧化态在酸性条件下不稳定易歧化?
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在酸性溶液中,Mn的元素电势图为:

(1)计算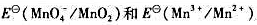 ;
;
(2)Mn的哪几种氧化态在酸性条件下不稳定易歧化?
 更多“在酸性溶液中,Mn的元素电势图为:(1)计算;(2)Mn的哪…”相关的问题
更多“在酸性溶液中,Mn的元素电势图为:(1)计算;(2)Mn的哪…”相关的问题
由附表六中查出酸性溶液中
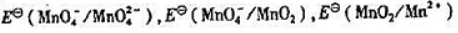
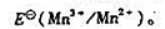
(1)颐出锰元素在酸性溶液中的元素电势图;
(2)计算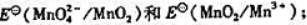
(3)MnO42-能否歧化?写出相应的反应方程式,并计算该反应的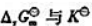 还有哪些物质能歧化?
还有哪些物质能歧化?
(4)计算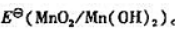
氯元素在酸性介质中的电势图为 HClO_____1.611V____Cl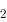 ____1.358V______Cl
____1.358V______Cl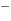 因为
因为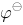 (HClO/Cl
(HClO/Cl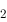 )>
)>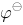 (Cl
(Cl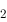 /Cl
/Cl ),所以Cl
),所以Cl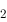 能发生歧化反应。()
能发生歧化反应。()
25℃时,Cu元素在酸性溶液中的元素标准电极电势图为
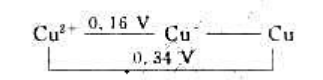
(1)试计算25℃时电对Cu2+/Cu的标准电极电势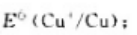
(2)已知2.303RT/F=0.060V,试计算25℃时Cu2+的歧化反应的标准平衡常数,
铬元素在酸性介质中的元素标准电极电势(ER/V)图为
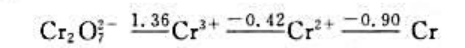
(1) 计算
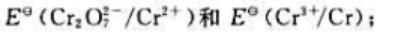
(2)判断Cr²+和Cr3+在酸性介质中是否发生歧化反应。
已知298K时,Mn元素在酸性溶液中的标准电极电势图如下:
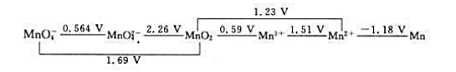
则298.15K、标准状态下,在酸性溶液中能发生歧化反应的是()。
A、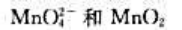
B、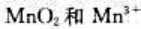
C、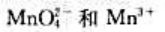
D、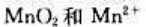
已知氯元素在碱性溶液中的元素电势图为: 则Eθ(ClO4-/ClO-)=________________V;Eθ(C103-/Cl2)=________________V;Eθ(ClO-/Cl-)=________________V;电势图中的物种,能自发进行歧化反应的_______________________。物种有________________________________________________。
根据锰元素的标准电势图讨论以下问题。
(1)计算Mn(Ⅲ)歧化反应的平衡常数,并说明歧化反应的趋势大小。
(2)MnO2-4稳定存在的条件,溶液的OH-浓度最低为多少?
300K时,Fe元素在酸性介质中的元素标准电极电势图为
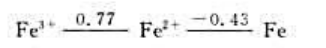
(1)计算300K时电对Fe3+/Fe在酸性介质中的标准电极电势;
(2)已知2.303RT/F=0.060V,计算反应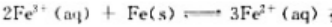 在300K时的标准平衡常数。
在300K时的标准平衡常数。
A.A.0.81V
B.B.1.51V
C.C.1.62V
D.D.1.05


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题