 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
臭氧分解
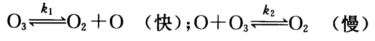 根据上述反应机理,如何用O3和O2的浓度表示它的速率方程?
根据上述反应机理,如何用O3和O2的浓度表示它的速率方程?
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
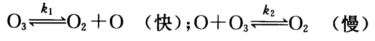 根据上述反应机理,如何用O3和O2的浓度表示它的速率方程?
根据上述反应机理,如何用O3和O2的浓度表示它的速率方程?
 更多“臭氧分解”相关的问题
更多“臭氧分解”相关的问题
有氧存在时,臭氧的分解机理为
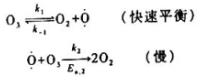
(1)分别导出用O3分解速率和O2生成速率所表示的速率方程,并指出二者关系.
(2)已知25℃时臭氧分解反应的表观活化能为119.2kJ·mol-1,O3和O的摩尔生成炜分别为
142.7kJ.mol-1和249.17kJ·mol-1,求上述第二步反应的活化能.
实验测得乙醛(CH3CHO)的热分解活化能为200.8kJ·mol-1,速率方程为:
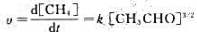
有人提出该分解反应机理为:
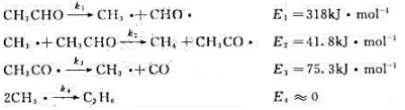
试推断上述反应机理是否合理,并求该反应的活化能.
A.零级反应
B.一级反应
C.二级反应
D.1.5级反应
已知反应2O3====3O2的反应机理为
O3====O2+O (慢)
O3+O====2O2(快)
当O2的浓度增加时,其反应速率
(A) 加快; (B) 减慢; (C) 基本保持不变; (D) 不能确定。
二氧化氮被臭氧化生成五氧化二氮.其反应机理如下:
①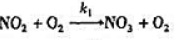 慢
慢
②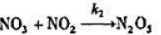 快
快
(1)写出反应方程式及其速率方程;
(2)写出各步反应的活化络合物的结构式及总反应的中间产物的化学式.
臭氧的分解反应为一级反应O3(g)→O2(g)+O(g),298K时的反应速率常数k=3×10-26s-1,则其半衰期t1/2=______。
A、CO + NO2 CO2 + NO ;
CO2 + NO ;
B、2NO2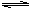
 2CO2 + 2NO (慢) ;
2CO2 + 2NO (慢) ;
C、2NO2 2NO + O2 (慢),2CO + O2
2NO + O2 (慢),2CO + O2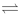 2CO2 (快) 。
2CO2 (快) 。
D、2NO2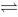 2NO + O2 (快),2CO + O2
2NO + O2 (快),2CO + O2 2CO2 (慢) 。
2CO2 (慢) 。


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题