 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
试求算0.15mol·dm-3氢氟酸中H+的浓度、体系的pH和氢氟酸的解离度。已知HF的Ka=6
.31x10-4。
提问人:网友18***469
发布时间:2022-01-07
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 更多“试求算0.15mol·dm-3氢氟酸中H+的浓度、体系的pH…”相关的问题
更多“试求算0.15mol·dm-3氢氟酸中H+的浓度、体系的pH…”相关的问题
说明可逆反应的速率常数k+、k-与其平衡常数K之间关系。若已知某温度下氢氟酸的解离反应
HF(aq)====H+(aq)+F-(aq)
平衡常数为7.08×10-4mol·dm-3,又已知基元反应
H+(aq)+F-(aq)====HF(aq)
的速率常数为1.00×1011dm3·mol-1·s-1,试求氢氟酸解离反应的速率常数。
在250ml.0.1mol·L-1HAc溶液中加入2.05gNaAc,求HAc的解离度和HAc溶液pH,已知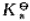 (HAc) =1.75×10-5。
(HAc) =1.75×10-5。
NH4Cl和NH3·H2O的混合溶液,其pH=9.5,已知NH3·H2O的的解离平衡常数为1.8x10^-5.。若溶液中NH4+浓度为5.0mol·dm-3,试求溶液[NH3·H2O]。
某一元弱酸HA的浓度为0.010mol·L-1,在常温下测得其pH为4.0。求该一元弱酸的解离平衡常数和解离度。
A.烧伤面积>1%BSA,氢氟酸浓度>50%
B.烧伤面积>5%BSA,任何浓度氢氟酸烧伤
C.吸入浓度在60%以上的氢氟酸烟雾
D.吸入浓度在30%以下的氢氟酸烟雾
将0.2mol·dm-3的HF与0.2mol·dm-3的KF溶液等体积混合,计算混合物的pH和HF的解离度?


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题