 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 更多“某溶液的pH值为1,此溶液中已无OH离子。”相关的问题
更多“某溶液的pH值为1,此溶液中已无OH离子。”相关的问题
已知某金属氢氧化物M(OH)2的Ksp=4×10-15,向0.10mol·L-1M2+溶液中加入NaOH,忽略体积变化和各种羟基络合物,计算下列不同情况生成沉淀时的pH值。
(1)M2+离子有1%沉淀
(2)M2+离子有50%沉淀
(3)M2+离子有99%沉淀
A.应在弱酸性溶液中进行
B.应在弱碱性溶液中进行
C.可在任意pH条件下进行
D.应在强碱性溶液中进行
已知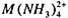 的lgβ1~lgβ4分别为2.0,5.0,7.0,10.0,M(OH)42-的lgβ1~lgβ4分别为4.0,8.0,14.0,15.0.在浓度为0.10mol.L-1的M2+溶液中,滴加氨水至溶液中的游离NH3浓度为0.010mol.L-1,pH=9.0.试问溶液中的主要存在形式是哪一种?浓度为多大?若将M2+离子溶液用NaOH和氨水调节至pH≈13.0且游离氨浓度为0.010mol.L-1,则上述溶液中的主要存在形式是什么?浓度又为多少?
的lgβ1~lgβ4分别为2.0,5.0,7.0,10.0,M(OH)42-的lgβ1~lgβ4分别为4.0,8.0,14.0,15.0.在浓度为0.10mol.L-1的M2+溶液中,滴加氨水至溶液中的游离NH3浓度为0.010mol.L-1,pH=9.0.试问溶液中的主要存在形式是哪一种?浓度为多大?若将M2+离子溶液用NaOH和氨水调节至pH≈13.0且游离氨浓度为0.010mol.L-1,则上述溶液中的主要存在形式是什么?浓度又为多少?
将50.0 mL 4.20 mol.dm-3氨水与50.0 mL 4.00 mol.dm-3HCl混合,计算在此混合溶液中: (1)[OH-]=? (2)溶液的PH=? (3)在此混合溶液中滴加Fe2+生成沉淀,则Fe(OH)2开始沉淀时的Fe2+离子浓度为多少?(Kbθ(NH3)=1.8×10-5,Kspθ[Fe(OH)2]=1.0×10-15)
已知某金属氢氧化物M(OH)2的Ksp=4×10-15,向0.10mol/L M2+溶液中加入NaOH,忽略体积变化和各种氢氧基络合物,计算下列不同情况生成沉淀时的pH值:(1)M2+有1%沉淀;(2)M2+有50%沉淀;(3)M2+有99%沉淀。
已知[M(NH3)4]2+的lgβ1~lgβ4分别为2.0、5.0、7.0、10.0,M(OH)4]2-的lgβ1~lgβ4分别为4.0、8.0、14.0、15.0。在浓度为0.10mol•L-1的M2+溶液中,滴加氨水至溶液中的游离NH3浓度为0.010mol•L-1,pH=9.0。试问溶液中的主要存在型体是哪一种?浓度为多大?若将M2+离子溶液用NaOH和氨水调节至pH≈13.0且游离氨浓度为0.010mol•L-1,则上述溶液中的主要存在型体是什么?浓度又为多少?

 如搜索结果不匹配,请
如搜索结果不匹配,请 






















