 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
反应2NO(g)+2H2(g)→N2(g)+2H2O(g)的反应速率方程为v=kc2(NO)c(H2),试讨论下列各种条件变化时对初速率有何影
反应2NO(g)+2H2(g)→N2(g)+2H2O(g)的反应速率方程为v=kc2(NO)c(H2),试讨论下列各种条件变化时对初速率有何影响。
(1)NO的浓度增加一倍;
(2)有催化剂参加;
(3)降低温度;
(4)将反应器的容积增大一倍;
(5)向反应体系中加入一定量的N2。
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
反应2NO(g)+2H2(g)→N2(g)+2H2O(g)的反应速率方程为v=kc2(NO)c(H2),试讨论下列各种条件变化时对初速率有何影响。
(1)NO的浓度增加一倍;
(2)有催化剂参加;
(3)降低温度;
(4)将反应器的容积增大一倍;
(5)向反应体系中加入一定量的N2。
 更多“反应2NO(g)+2H2(g)→N2(g)+2H2O(g)的…”相关的问题
更多“反应2NO(g)+2H2(g)→N2(g)+2H2O(g)的…”相关的问题
A、反应级数为2,反应分子数为3
B、反应级数为2,反应分子数为2
C、反应级数为2,不存在反应分子数
D、反应级数与反应分子数均不存在
A、pV=nRT
B、p(H2)V=n(H2)RT
C、p(H2)V(H2)=n(H2)RT
D、pV(N2)=n(N2)RT
(1)3H2(g)+N2(g)→2NH3(g)
(2)3/2H2(g)+1/2N2(g)→NH3(g)
(3)H2(g)+1/3N2(g)→2/3NH3(g)bi
应进度ξ=0.5mol则.上述三个反应方程可生成的NH3的物质的量比为:()。
A、1:1:1
B、1:0.5:0.33
C、2:1:0.66
D、不能确定
22. No与H2进行的反应为2NO(g)+2H2(g)→N2(g)+2H2O(g)。在一定温度下,某密闭容器中等摩尔比的NO与H2混合物在不同初压下的半衰期如表11-20所示,求反应的总级数n。
表11-20
|
A. 向生成NO2的方向进行
B. 正好达到平衡
C. 难以判断其进行的方向
D. 向生成N2O4的方向进行
A、-dc(SO2)/2dt
B、2dc(SO3) / dt
C、-2dc(SO2) / dt
D、-dc(SO2) / dt
对于基元反应:NO (g)+CO(g)=NO(g)+CO
(g)+CO(g)=NO(g)+CO (g)其反应速率常数k的单位是( )
(g)其反应速率常数k的单位是( )
A、s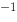
B、L ·mol
·mol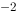 ·s
·s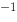
C、mol·L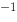 ·s
·s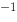
D、L·mol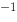 ·s
·s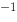
若 CH4 (g),CO2 (g),H2O(l) 的 分别为 -50.8, -394.4, -237.2 kJ·mol-1,则 298 K时 ,CH4 (g) + 2O2 (g) → CO2 (g) + 2H2O(l) 的
分别为 -50.8, -394.4, -237.2 kJ·mol-1,则 298 K时 ,CH4 (g) + 2O2 (g) → CO2 (g) + 2H2O(l) 的 (kJ·mol-1)为
(kJ·mol-1)为
A、-818
B、818
C、-580.8
D、580.8
B.双分子反应,二级反应
C.一级反应
D.二级反应
E.三分子反应、二级反应


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题