 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
质量为m 的氢气() 处于温度T的平衡态时,1mol该气体的内能是:
A.3kT/2
B.5kT/2
C.3RT/2
D.5RT/2
提问人:网友lixin080108
发布时间:2022-01-07
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.3kT/2
B.5kT/2
C.3RT/2
D.5RT/2
 更多“质量为m 的氢气() 处于温度T的平衡态时,1mol该气体的…”相关的问题
更多“质量为m 的氢气() 处于温度T的平衡态时,1mol该气体的…”相关的问题
A、(1)-4.3kJ (2)0 (3)-2.3kJ
B、1
C、3
D、5

A、分子的平均平动动能为 kT/2
B、分子的平均平动动能为 3 kT/2
C、分子的平均平动动能为 i kT/2
D、分子的平均动能为 i kT/2
E、内能为 N i kT/2
F、分子的平均转动动能 (i-3)kT/2
【单选题】理想气体处于平衡状态,设温度为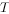

A、每个气体分子所具有的动能为
B、每个气体分子所具有的动能为
C、每个气体分子所具有的平均动能为
D、1mol气体分子所具有的平均能量为


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题