 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
反应2SO2(g)+O2(g)=2SO3(g)在298K时标准平衡常数KӨ=6.3×1024,若在此温度时,该反应式中的各物质均处于标准状态,则反应进行的方向是:()。
A、处于平衡状态
B、逆向进行
C、正向进行
D、无法判断
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A、处于平衡状态
B、逆向进行
C、正向进行
D、无法判断
 更多“反应2SO2(g)+O2(g)=2SO3(g)在298K时标…”相关的问题
更多“反应2SO2(g)+O2(g)=2SO3(g)在298K时标…”相关的问题
A.处于平衡状态
B.逆向进行
C.正向进行
D.无法判断
反应CO(g)+H2O(g)===CO2(g)+H2(g)在700℃时的标准平衡常数KΘ=0.71。当各物质的分压力均为0.1MPa时,该反应在700℃时的△rGm=______。
反应Zn2+(1×10-5molL-1)+Cu=Zn+Cu2+(0.1 molL-1)在298K时标准平衡常数KΘ约等于()。已知:φΘ(Zn2+/Zn)=-0.76V,φΘ(Cu2+/Cu)=0.34V。
A.1037
B.1042
C.10-37
D.10-42
计算题:合成氨的反应式为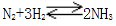 ,在400℃时,反应达到平衡,各物质的平衡浓度为:[N2]=3mol/L,[H2]=9=3mol/L,[NH3]=4mol/L。求在该温度下的平衡常数Kc、Kp以及N2和H2的原始浓度。
,在400℃时,反应达到平衡,各物质的平衡浓度为:[N2]=3mol/L,[H2]=9=3mol/L,[NH3]=4mol/L。求在该温度下的平衡常数Kc、Kp以及N2和H2的原始浓度。
已知反应A (g) = B (g) + C (g) 各物质在298K时的热力学数据如下: 物 质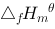 (298k)/
(298k)/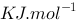 A (g) –235.30 B (g) 52.28 C (g) –241.80 求该反应的标准摩尔反应焓
A (g) –235.30 B (g) 52.28 C (g) –241.80 求该反应的标准摩尔反应焓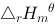 和标准摩尔热力学能变
和标准摩尔热力学能变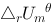 .
.
某一气相反应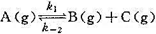 ,已知在298 K时,k1=0.21s-1,k-2=5×10-9Pa-1·s-1,当温度由298 K升到310 K时,k和k-2的值均增加1倍,试求:
,已知在298 K时,k1=0.21s-1,k-2=5×10-9Pa-1·s-1,当温度由298 K升到310 K时,k和k-2的值均增加1倍,试求:
(1)298K时的反应平衡常数Kp;
(2)正、逆反应的实验活化能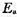 ;
;
(3)298K时反应的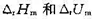 ;
;
(4)在298K时,A的起始压力为100kPa,若使总压力达到152kPa,所需的时间。
在454~475K温度范围内,反应2C2H5OH(g)===CH3COOC2H5(g)+2H2(g)的标准平衡常数KΘ与T的关系为 。已知473K时,乙醇的
。已知473K时,乙醇的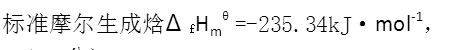 。求该温度时乙酸乙酯的
。求该温度时乙酸乙酯的 。
。
298K时,Ag(s)|Ag+(a)的标准电极电势EΘ=0.799V,反应Fe3+(a2)+Ag(s)→Fe2+(a3)+Ag+(a1)的平衡常数KΘ=0.531,试求
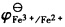 。
。
A.热力学平衡常数与反应体系中各物质的活度有关,对一个反应体系来说,当其内物质的活度发生变化时该反应的热力学平衡常数也会发生变化;
B. 热力学平衡常数与反应体系中各物质的活度无关,但可以用反应达到平衡时体系内各物质的平衡活度进行计算;
C. 热力学平衡常数与温度无关,但可以用标准状态下反应的吉布斯自由能变进行计算;
D. 水的离子积KW实际上就是水离解反应的热力学平衡常数。


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题