 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
下列选项中,对“休克尔规则”描述不正确的是
A.n是指环碳原子数
B.分子必须是环状的和平面的
C.环原子可以有sp3杂化原子中断这个离域的π电子体系
D.π 电子总数必须等于4n+2
提问人:网友seven741
发布时间:2022-01-07
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.n是指环碳原子数
B.分子必须是环状的和平面的
C.环原子可以有sp3杂化原子中断这个离域的π电子体系
D.π 电子总数必须等于4n+2
 更多“下列选项中,对“休克尔规则”描述不正确的是”相关的问题
更多“下列选项中,对“休克尔规则”描述不正确的是”相关的问题
A.体系必须是平面环状结构。
B.成环的原子必须有未杂化的p轨道,用以形成共轭p键。
C.成环原子的p电子数等于4n+2(n=0,1,2,3...)。
D.成环原子必须是碳原子。
E.判段对象必须是中性分子,不能是离子。
休克尔分子轨道理论中休克尔行列式(注: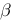 没有移到分母项时)有以下几个特点:
没有移到分母项时)有以下几个特点:
A、行列式的阶由参加离域大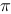 键的原子数决定
键的原子数决定
B、行列式的主对角元为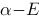
C、行列式的非对角元为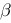 和0,且
和0,且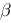 的分布总是紧挨着主对角元
的分布总是紧挨着主对角元
D、如有杂原子参加, 诸 须分别标记清楚
须分别标记清楚


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题