 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
30.0mL 0.150mol/L的HCl溶液和20.0mL 0.150mol/L的Ba(OH)2溶液相混合,所得溶液是酸性、中性、还是碱性?计算过
30.0mL 0.150mol/L的HCl溶液和20.0mL 0.150mol/L的Ba(OH)2溶液相混合,所得溶液是酸性、中性、还是碱性?计算过量反应物的浓度。
提问人:网友anonymity
发布时间:2022-01-06
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
30.0mL 0.150mol/L的HCl溶液和20.0mL 0.150mol/L的Ba(OH)2溶液相混合,所得溶液是酸性、中性、还是碱性?计算过量反应物的浓度。
 更多“30.0mL 0.150mol/L的HCl溶液和20.0mL…”相关的问题
更多“30.0mL 0.150mol/L的HCl溶液和20.0mL…”相关的问题
A、无色
B、蓝色
C、红色
D、红棕色
A、无沉淀析出
B、有沉淀析出
C、析出沉淀后又溶解
D、不一定
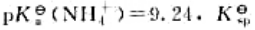 (Fe(OH)3)=2.79×10-39)
(Fe(OH)3)=2.79×10-39)
称取Na2HPO4·12H2O试剂0.8835g,以甲基橙为指示剂,用0.1012mol/L HCl滴定至H2PO4-,消耗HCl溶液27.30mL。计算样品中Na2HPO4·12H2O的质量分数,并解释所得结果。
市售浓盐酸的密度为1.19g/cm3,质量分数为36.5%,用此盐酸配制250mL 0.1mol/L的HCl溶液,应取浓盐酸多少毫升?
用0.10mol/L HCl标准溶液滴定0.10mol/L NaX(HX的Ka=5.0×10-10)。试问:能否准确滴定?并写出计算过程;若能准确滴定,计算化学计量点时的pH值?能用酚酞或甲基橙做指示剂吗?


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题