 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
25℃时,电极反应O2+2H++2e-====H2O2的标准电极电势为0.68V,已知φ=0.401V,则电极反应H2O2+2H++2e-====2H2O的标准电极电势为( )
A.0.2576V
B.0.279V
C.1.081V
D.1.777V
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.0.2576V
B.0.279V
C.1.081V
D.1.777V
 更多“25℃时,电极反应O2+2H++2e-====H2O2的标准…”相关的问题
更多“25℃时,电极反应O2+2H++2e-====H2O2的标准…”相关的问题
已知25°C时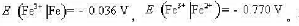 试计算应25°C时电极Fe2+|Fe的标电极电势E(Fe2+|Fe)。
试计算应25°C时电极Fe2+|Fe的标电极电势E(Fe2+|Fe)。
101.3kPa,25℃下,下列反应的反应焓为5.36kJ·mol-1:
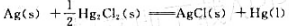
已知25℃时,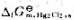 =-210.7kJ·mol-1,
=-210.7kJ·mol-1,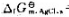 =-109.7kJ·mol-1,请:
=-109.7kJ·mol-1,请:
(1)试为上述反应设计一可逆电池,写出电池表示式和电极反应;
(2)求所设计电池的电动势及其温度系数和电池反应的ΔtGmθ、ΔtSmθ:
(3)求25℃时,电极C1-|Hg2Cl2|Hg的标准电极电位;
已知25℃时,Eθ[Ag+|AgCl(s)|Ag]=0.2224V
(4)已知25℃时Eθ(Hg22+|Hg)=0,798V,求Hg2Cl2在25℃时的溶度积.
A、在任何温度下,标准氢电极的电极反应的电势都为零;
B、在25℃时,标准氢电极的电极反应的电势才为零;
C、在任何温度下,标准氢电极的电极反应的电势都不为零
A.在任何温度下,标准氢电极的电极反应的电势都为零
B.在 25 ℃ 时,标准氢电极的电极反应的电势才为零
C.在任何温度下,标准氢电极的电极反应的电势都不为零
在25℃时测定某一电极反应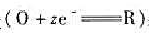 得下列数据:
得下列数据:

平均极限扩散电流为3.24mA,求:
(1)电极反应的转移电子数;
(2)电极反应是否可逆;
(3)假定氧化态和还原态的活度系数和扩散系数相等,计算氧化还原体系的标准电位(相对于SCE)。
5.写出下列原电池的电极反应式和电池反应式,并计算25℃时原电池的电动势。
Fe|Fe2+(1.0mol/L)||Cl-(1.0mol/L)|Cl2(100kpa),Pt
A.25;1.0
B.37;1.0
C.25;0
D.37;0
将反应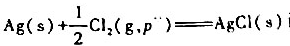 设计成原电池.已知25°C;时,
设计成原电池.已知25°C;时,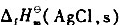 =-127.07kJ.mol-1.
=-127.07kJ.mol-1.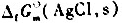 =-109.79kJ.mol-1,标准电极电势
=-109.79kJ.mol-1,标准电极电势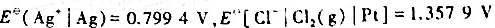 .
.
(1)写出电极反应和电池图示;
(2)求25°C、电池可逆放电2F电荷悬时的热Qz;
(3)求25°C时AgCl的活度积Kap.


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题