 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
25℃时二元弱酸H2B的试计算: (1)25℃时0.10mol·L-1H2B溶液的pH; (2)25℃时0.10
25℃时二元弱酸H2B的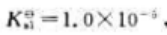
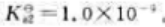
试计算:
(1)25℃时0.10mol·L-1H2B溶液的pH;
(2)25℃时0.10mol·L-1NaHB溶液的pH;
(3)25℃时0.10mol·L-1.H2B0.010mol·L-1NaHB混合溶液的pH:
(4)25℃时0.10mol·L-1Na2B溶液的pH。
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
25℃时二元弱酸H2B的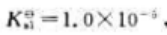
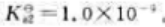
试计算:
(1)25℃时0.10mol·L-1H2B溶液的pH;
(2)25℃时0.10mol·L-1NaHB溶液的pH;
(3)25℃时0.10mol·L-1.H2B0.010mol·L-1NaHB混合溶液的pH:
(4)25℃时0.10mol·L-1Na2B溶液的pH。
 更多“25℃时二元弱酸H2B的试计算: (1)25℃时0.10mo…”相关的问题
更多“25℃时二元弱酸H2B的试计算: (1)25℃时0.10mo…”相关的问题
H2B为二元弱酸,pH=1.92时,δH2B=δHB-;pH=6.22时,δHB-=δB2-,计算(1)H2B的KA1和KA2;(2)当pH的值为多少时,二元弱酸以HB-的形式存在;(3)用0.100mol/L NaOH溶液滴定0.100mol/L H2B,滴定至第一和第二化学计量点时,溶液的pH值为多少?各选何种指示剂?
已知二元弱酸H2B的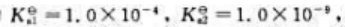 则二元弱碱B的K为().
则二元弱碱B的K为().
A、1.0×10-4
B、1.0×10-9
C、1.0×10-5
D、1.0×10-4
25℃时,一元弱酸HA的标准解离常数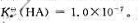 试计算0.10mol·L-1HA溶液的pH和HA的解离度。
试计算0.10mol·L-1HA溶液的pH和HA的解离度。
A.[H+]=2c mol/L
B.[B2-]=c mol/L
C.[H2B]=c mol/L
D.[H2B]+[HB-]+[B2-]=c mol/L
A.2.0×10-10
B.5.0×10-14
C.3.2×10-8
D.2.0×10-16
水杨酸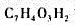 有时可作为止痛药而代替阿司匹林,它是二元弱酸。计算0.10mol/L水杨酸溶液中各离子浓度和pH。
有时可作为止痛药而代替阿司匹林,它是二元弱酸。计算0.10mol/L水杨酸溶液中各离子浓度和pH。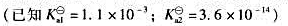


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题