 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
5. 1 mol O2处于25℃、101325 Pa下,试计算O2分子的平动配分函数。(已知O2的摩尔质量为32.00 g·mol,k = 13.81 ´ 10-24 J·K-1,h = 0.6626 ´ 10-33 J·s。)
提问人:网友besthool889
发布时间:2022-01-07
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 更多“5. 1 mol O2处于25℃、101325 Pa下,试计…”相关的问题
更多“5. 1 mol O2处于25℃、101325 Pa下,试计…”相关的问题
O2(g)的摩尔定压热容与温度的函数关系为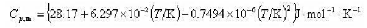 已知25°C下O2(g)的标准摩尔熵Sm=205.138J·mol-1·K-1.求O2(g)在100°C50kPa下的摩尔规定熵值Sm。
已知25°C下O2(g)的标准摩尔熵Sm=205.138J·mol-1·K-1.求O2(g)在100°C50kPa下的摩尔规定熵值Sm。
已知O2(g)的摩尔定压热容与温度的函数关系为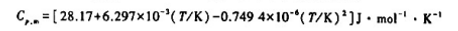 ,且25℃时O2(g)的标准摩尔熵
,且25℃时O2(g)的标准摩尔熵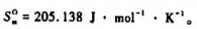 求O2(g)在100℃,50kPa下的摩尔规定熵值Sm.
求O2(g)在100℃,50kPa下的摩尔规定熵值Sm.
A.1.883×105 kg
B.1.883×106 kg
C.1.883×107 kg
D.1.883×108 kg
质量相同的氢气(H2)和氧气(O2),处在相同的室温下,则它们的分子平均平动动能和内能的关系是: A.分子平均平动动能相同,氢气的内能大于氧气的内能 B.分子平均平动动能相同,氧气的内能大于氢气的内能 C.内能相同,氢气的分子平均平动动能大于氧气的分子平均平动动能 D.内能相同,氧气的分子平均平动动能大于氢气的分子平均平动动能
在101.33kPa、0℃下的O2与CO混合气体中发生稳定的分子扩散过程。已知相距0.2cm的两截面上O2的分压分别为13.33kPa和6.67kPa,又知扩散系数为0185cm2/s,试计算下列两种情况下O2的传递速率,kmol/(m2·s):



为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题