 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
以K2Cr2O7标准溶液滴定Fe2+,计算25℃时反应的平衡常数;若化学计量点时Fe3+的浓度为0.05000mol·L-1,要使反应
以K2Cr2O7标准溶液滴定Fe2+,计算25℃时反应的平衡常数;若化学计量点时Fe3+的浓度为0.05000mol·L-1,要使反应定量进行,所需H+的最低浓度为多少?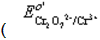
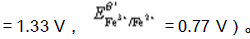
提问人:网友anonymity
发布时间:2022-01-07
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
以K2Cr2O7标准溶液滴定Fe2+,计算25℃时反应的平衡常数;若化学计量点时Fe3+的浓度为0.05000mol·L-1,要使反应定量进行,所需H+的最低浓度为多少?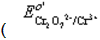
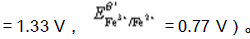
 更多“以K2Cr2O7标准溶液滴定Fe2+,计算25℃时反应的平衡…”相关的问题
更多“以K2Cr2O7标准溶液滴定Fe2+,计算25℃时反应的平衡…”相关的问题
A、次甲基蓝(φ0‘=0.36V)
B、二苯胺磺酸钠(φ0‘=0.84V)
C、邻二氮菲亚铁(φ0‘=1.06V)
D、二苯胺(φ0‘=0.76V)
A. 配制NA、OH标准液时,用量筒取水
B. 以K2C、r2O7标定NA、2S2O3时,在近终点时才加淀粉指示剂
C. 配制KMnO4标准液时,用台秤称量KMnO4固体
D. 用邻苯二甲酸氢钾作基准物质标定HC、l溶液
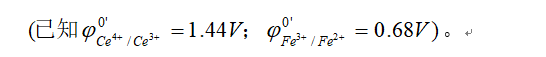


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题