 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
已知下列半电池反应及其标准电极电位为计算络合物平衡反应:的不稳定常数。(25℃)
已知下列半电池反应及其标准电极电位为计算络合物平衡反应:的不稳定常数。(25℃)
已知下列半电池反应及其标准电极电位为
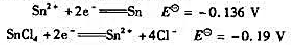
计算络合物平衡反应:
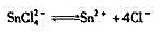 的不稳定常数。(25℃)
的不稳定常数。(25℃)
提问人:网友yr1161772517
发布时间:2022-01-07
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知下列半电池反应及其标准电极电位为
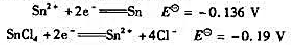
计算络合物平衡反应:
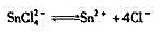 的不稳定常数。(25℃)
的不稳定常数。(25℃)
 更多“已知下列半电池反应及其标准电极电位为计算络合物平衡反应:的不…”相关的问题
更多“已知下列半电池反应及其标准电极电位为计算络合物平衡反应:的不…”相关的问题
将氧化还原反应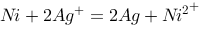 设计为一个原电池,已知
设计为一个原电池,已知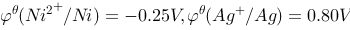 ,则原电池的电动势
,则原电池的电动势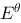 为1.05 (V),
为1.05 (V),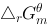 为-203 kJ/mol,该氧化还原反应的平衡常数为
为-203 kJ/mol,该氧化还原反应的平衡常数为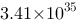 。
。
(a)哪一个共轭电对有较大失去电子的倾向?
(b)哪一个共轭电对有较强的氧化能力?
(c)如果在pH7时,每一反应物和生成物的浓度为1M,试问下列反应进行的方向。丙酮酸+NADH+H+=乳酸+NAD+
(d)在25℃,此反应的标准自由能的变化ΔG°†。
(e)在25℃,此反应的平衡常数?
A、前轴≤24%
B、前轴≤20%
C、后轴≤30%(轴制动力大于等于该轴轴荷60%时)
D、后轴≤10%(轴制动力小于该轴轴荷60%时)


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题