 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
若850℃时,反应CaCO3(s)
若850℃时,反应CaCO3(s) CaO(s)+CO2(g)Kө=0.498,则平衡时CO2分压为
CaO(s)+CO2(g)Kө=0.498,则平衡时CO2分压为
A.50.5kPa
B.0.498kPa
C.71.5kPa
D.取决于CaCO3的量
提问人:网友yyokok
发布时间:2022-01-07
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 CaO(s)+CO2(g)Kө=0.498,则平衡时CO2分压为
CaO(s)+CO2(g)Kө=0.498,则平衡时CO2分压为A.50.5kPa
B.0.498kPa
C.71.5kPa
D.取决于CaCO3的量
 更多“若850℃时,反应CaCO3(s) [图]CaO(s)+CO…”相关的问题
更多“若850℃时,反应CaCO3(s) [图]CaO(s)+CO…”相关的问题
800℃下,CaCO3(s)分解反应CaCO3(s)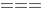 CaO(s) + CO2(g) 达到平衡,系统的相数P=( )。
CaO(s) + CO2(g) 达到平衡,系统的相数P=( )。
A、0
B、1
C、2
D、3

A、CaO (s) +CO2 (g) = CaCO3 (s)
B、2 AgNO3 (s) = 2 Ag (s) + 2 NO2 (g) + O2 (g)
C、CaCO3 (s) = CaO (s) + CO2 (g)
D、2 NO (g) = N2 (g) + O2 (g)
 。若将1.00 mol CaCO3装入1.00 dm3真空容器中,加热到1500 K达平衡时,气体混合物中O2的摩尔分数为0.15。计算容器中CaO的物质的量n(CaO)。
。若将1.00 mol CaCO3装入1.00 dm3真空容器中,加热到1500 K达平衡时,气体混合物中O2的摩尔分数为0.15。计算容器中CaO的物质的量n(CaO)。
A、5.29×10-4 mol/L
B、5.29 ×10-5 mol/L
C、1.67×10-5 mol/L
D、1.67×10-4 mol/L
A、C=3;P=3;F=2
B、C=2;P=3;F=1
C、C=1;P=3;F=0
D、C=2;P=2;F=2
N2(g)+3H2(g)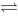 2NH3(g),反应达到平衡后,把PNH3,PH2各提高到原来的2倍,PN2不变,则平衡将会
2NH3(g),反应达到平衡后,把PNH3,PH2各提高到原来的2倍,PN2不变,则平衡将会
A、向正反应方向移动
B、向逆反应方向移动
C、状态不变
D、无法确知


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题