 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知pH=2.00,则[H+]为()mol/LA.0.01B.0.010C.0.0100D.0.01000
已知pH=2.00,则[H+]为()mol/L
A.0.01
B.0.010
C.0.0100
D.0.01000
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知pH=2.00,则[H+]为()mol/L
A.0.01
B.0.010
C.0.0100
D.0.01000
 更多“已知pH=2.00,则[H+]为()mol/LA.0.01B…”相关的问题
更多“已知pH=2.00,则[H+]为()mol/LA.0.01B…”相关的问题
已知Cd2+的一级水解反应:Cd2++H2O=Cd(OH)++H+的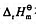 在298.15K为60kJ·mol-1,
在298.15K为60kJ·mol-1,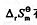 在298.15K为20J·mol-1·K-1。试求298.15K时,此水解反应的标准平衡常数以及0.10mol·dm-3的Cd(NO3)2溶液的pH[设Cd(NO3)2在水溶液中完全电离或解离]。
在298.15K为20J·mol-1·K-1。试求298.15K时,此水解反应的标准平衡常数以及0.10mol·dm-3的Cd(NO3)2溶液的pH[设Cd(NO3)2在水溶液中完全电离或解离]。
100mLpH=2.00的[c(H+)=10-2]某强电解质溶液和等体积pH=13.00的强电解质溶液[c(OH-)=10-1]混合,pH与下列数据最近的是( )。
(A) 7.5 (B) 12.65 (C) 12.95 (D) 6.5
将pH=2.00和pH=3.00的盐酸溶液等体积混合。近似计算混合液pH时,有以下两种方法:
方法1:
溶液(1)中:c(H+)=1.00×10-2mol·L-1
溶液(2)中:c(H+)=1.00×10-3mol·L-1
混合后:c(H+)=5.5×10-3mol·L-1
pH=2.26
方法2:
溶液(1)中:c(OH-)=1.00×10-12mol·L-1
溶液(2)中:c(OH-)=1.00×10-11mol·L-1
混合后:c(OH-)=5.5×10-3mol·L-1
pOH=11.26,pH=2.74
所得结果不同。哪种方法正确?为什么?
经检验,某酸雨的成分除含有少量H+和极少量OH-外,还有Na+、Cl-、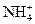 、 、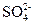 等离子,已知:c(Na+)=7×10-6mol· L-1,c(Cl-)=3.5×10-5mol· L-1,c( 等离子,已知:c(Na+)=7×10-6mol· L-1,c(Cl-)=3.5×10-5mol· L-1,c(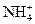 )=2.3×10-5mol· L-1,c( )=2.3×10-5mol· L-1,c(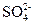 ) =2.5×10-6mol·L-1,则该酸雨的pH为() ) =2.5×10-6mol·L-1,则该酸雨的pH为()
|
A、2.2 mol
B、1.1 mol
C、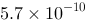 mol
mol
D、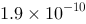 mol
mol
A、2.2 mol
B、1.1 mol
C、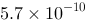 mol
mol
D、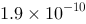 mol
mol
A.2.2 mol
B.1.1mol
C.5.7×10-10mol
D.1.9×10-10


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题