 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
现有25°C时,0.01mol●kg-1的BaCl2水溶液.计算溶液的离子强度I及BaCl2的平均离子
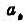 .
. 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
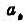 .
. 更多“现有25°C时,0.01mol●kg-1的BaCl2水溶液.…”相关的问题
更多“现有25°C时,0.01mol●kg-1的BaCl2水溶液.…”相关的问题
若质量摩尔浓度均为0.001mol·kg-1的NaCl,BaCl2,CaSO4溶液的离子平均活度因子(系数)分别为γ±(NaCl),γ±(BaCl2),γ±(CaSO4),请排出三者γ±由大到小的次序为______。
0.01mol/kg的BaCl2和0.005mol/kg的La(NO)3混合溶液的离子强度I=______。
01mol/kg的BaCl2和0.005mol/kg的La(NO)3混合溶液的离子强度I=_______。
25℃时,AgCI的溶度积K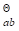 =1.71×10-10,试求在饱和水溶液中.AgCI的离子平均活度及离子平均活度系数各为多少?
=1.71×10-10,试求在饱和水溶液中.AgCI的离子平均活度及离子平均活度系数各为多少?
在25℃的水溶液中,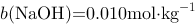 ,其正负离子的平均离子活度因子
,其正负离子的平均离子活度因子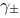 =0.899,则正负离子的平均活度
=0.899,则正负离子的平均活度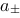 ()。
()。
A、0.899
B、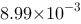
C、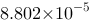
D、0.01
有下列不同类型的电解质: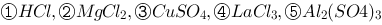 ,设它们都是强电解质,当它们的溶液质量摩尔浓度都是0.025
,设它们都是强电解质,当它们的溶液质量摩尔浓度都是0.025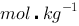 时,试计算各种溶液的: (1)离子强度I; (2)离子平均质量摩尔浓度
时,试计算各种溶液的: (1)离子强度I; (2)离子平均质量摩尔浓度 ; (3)用Debye-Hückel极限公式计算离子平均活度因子
; (3)用Debye-Hückel极限公式计算离子平均活度因子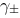 ; (4)电解质的离子平均活度
; (4)电解质的离子平均活度 和电解质的活度
和电解质的活度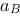 。
。
首先计算0.0015mol·-1MgCl2水溶液的离子强度;然后用德拜极限方程计算:(1) Mg2+,Cl-的活度系数;(2) 平均活度系数。(298K)


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题