 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
已知在1.0mol·dm-3H2SO4溶液中,电对MnO4-/Mn2+和电对Fe3+/Fe2+的条件电极电势分别为1.45V和0.68V,在此条件下用KMnO4标准溶液滴定Fe2+,其等当点的电势值为( )。
A.0.38V
B.0.73V
C.0.89V
D.1.32V
提问人:网友anonymity
发布时间:2022-01-07
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.0.38V
B.0.73V
C.0.89V
D.1.32V
 更多“已知在1.0mol·dm-3H2SO4溶液中,电对MnO4-…”相关的问题
更多“已知在1.0mol·dm-3H2SO4溶液中,电对MnO4-…”相关的问题
A、1.06V
B、1.44V
C、0.85V
D、0.68V
反应Sn2++2Fe2+=Sn4++2Fe2+能自发进行,将其设计为原电池,电池符号为:()

A. A
B. B
C. C
D. D
298.15K标准状态下,反应[Cu(CN)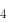 ]
]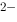 +4H
+4H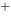 = 4HCN + Cu
= 4HCN + Cu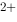 自发进行的方向应为( )。(已知298.15K时,
自发进行的方向应为( )。(已知298.15K时,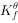
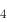 ]
]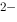 }=2.0×10
}=2.0×10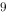 ,
,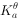
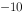 )
)
A、正向
B、逆向
C、平衡
D、三种情况都有可能
(1)计算理论分解电压;
(2)若两电极面积均为1cm2,电解液电阻为100Ω,H2(g)和O2(B)的超电势η与电流密度J的关系分别为

问当通过的电流为1mA时,外加电压为若干?
A、3.00 mg/L
B、30.03mg/L
C、300.30 mg/L
D、0.30 mg/L


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题