 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
电动势E(或电极电势φ)的数值与反应式(或半反应式)的写法无关,而标准平衡常数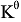 的数值随反应式的写法(即化学计量数不同)而变。 ( )
的数值随反应式的写法(即化学计量数不同)而变。 ( )
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 更多“电动势EΘ(或电极电势φ)的数值与反应式(或半反应式)的:写…”相关的问题
更多“电动势EΘ(或电极电势φ)的数值与反应式(或半反应式)的:写…”相关的问题
电动势E(或电极电势φ)的数值与反应式(或半反应式)的写法无关,而标准平衡常数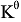 的数值随反应式的写法(即化学计量数不同)而变。 ( )
的数值随反应式的写法(即化学计量数不同)而变。 ( )
A.有两个原电池,测得其电动势相等,这表明两原电池中反应的△GӨ值也相等;
B.越大的电极电势值电对,其氧化态物质的氧化性越强;
C.原电池的能量变化是由化学能变为电能,原电池的正极是阴极,发生还原反应;
D.电极电势的数值与电极反应的写法无关,而平衡常数的数值随反应式的写法而变。
(1)写出原电池符号、电池反应式;
(2)查标准电极电势表,求该原电池的标准电动势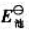 ;
;
(3)当电池反应进行到c(Cu2+)=1.0mol·dm-3时,试计算原电池的电动势E池。
(1)写出下列各电对的电极反应式,并根据元素电势图给出各电极反应的标准电极电势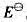 。
。
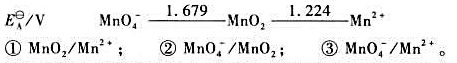
(2)试写出以电对①为负极、电对②为正极的原电池的电池反应,并计算原电池的标准电动势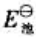 和电池反应的
和电池反应的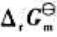 。
。
(3)试写出以电对①为负极、电对③为正极的原电池的电池反应,并计算原电池的标准电动势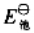 和电池反应的
和电池反应的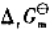 。
。
由标准钴电极(Co2+/Co)与标准氯电极组成原电池,测得其电动势为1.64V,此时钴电极为负极。已知 (Cl2/Cl-)=1.36V。问:(1) 标准钴电极的电极电势为多少(不查表)?(2) 此电池反应的方向如何?(3) 当氯气的压力增大或减小时,原电池的电动势将发生怎样的变化?(4) 当Co2+的浓度降低到0.010mol·dm-3时,原电池的电动势将发生怎样的变化?数值是多少?
(Cl2/Cl-)=1.36V。问:(1) 标准钴电极的电极电势为多少(不查表)?(2) 此电池反应的方向如何?(3) 当氯气的压力增大或减小时,原电池的电动势将发生怎样的变化?(4) 当Co2+的浓度降低到0.010mol·dm-3时,原电池的电动势将发生怎样的变化?数值是多少?
A.()标准氢电极‖待测电极(-)
B.(-)待测电极‖标准氢电极()
C.(-)标准氢电极‖待测电极()
D.()待测电极‖标准氢电极(-)
假设规定标准氢电极的电极电势 (H+/H2)=1v,则测得下列原电池(一)Zn|Zn2+(1mol·dm-3)||H+(1mol·dm-3)|H2(p)|Pt()的标准电动势
(H+/H2)=1v,则测得下列原电池(一)Zn|Zn2+(1mol·dm-3)||H+(1mol·dm-3)|H2(p)|Pt()的标准电动势 和锌标准电极电势
和锌标准电极电势 (Zn2+/Zn)的数值变化为()。
(Zn2+/Zn)的数值变化为()。
A.标准电动势 和锌标准电极电势
和锌标准电极电势 (Zn2+/Zn)各增加1V
(Zn2+/Zn)各增加1V
B.标准电动势 和锌标准电极电势
和锌标准电极电势 (Zn2+/Zn)各减少1V
(Zn2+/Zn)各减少1V
C.标准电动势 不变,锌标难电极电势
不变,锌标难电极电势 (Zn2+/Zn)增加1V
(Zn2+/Zn)增加1V
D.标准电动势 不变,锌标准电极电势
不变,锌标准电极电势 (Zn2+/Zn)减少1V
(Zn2+/Zn)减少1V
E.标准电动势 和锌标准电极电势
和锌标准电极电势 (Zn2+/Zn)均不变
(Zn2+/Zn)均不变


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题