 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
处理一定量的SO2水溶液时,消耗某KMnO4标液20.00mL,该反应所产生的酸需用0.1000mol/L NaOH溶液20.00mL才能完全中和;若用此KMnO4滴定某H2O2溶液(密度1.010g/mL),10.00mL H2O2需消耗38.00mL KMnO4溶液,问H2O2溶液的质量分数为多少?(H2O2的相对分子质量为34.02)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 更多“10.00mL市售H2O2(相对密度1.010)需用36.8…”相关的问题
更多“10.00mL市售H2O2(相对密度1.010)需用36.8…”相关的问题
处理一定量的SO2水溶液时,消耗某KMnO4标液20.00mL,该反应所产生的酸需用0.1000mol/L NaOH溶液20.00mL才能完全中和;若用此KMnO4滴定某H2O2溶液(密度1.010g/mL),10.00mL H2O2需消耗38.00mL KMnO4溶液,问H2O2溶液的质量分数为多少?(H2O2的相对分子质量为34.02)
市售的试剂浓硫酸的浓度为98%,密度为1.84g·mL-1,配制1.25dm3浓度为3.0mol·dm-3的硫酸溶液,需用浓硫酸多少毫升?
配制0.1mol∕L盐酸溶液1000mL,需用密度为ρ=1.19g∕cm3、质量分数为37.23﹪的浓盐酸()mL。
相对密度为1.01的含3.00%的H2O2溶液2.50mL,与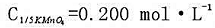 的KMnO4溶液完全作用,需此浓度的KMnO4溶液多少毫升?已知滴定反应为
的KMnO4溶液完全作用,需此浓度的KMnO4溶液多少毫升?已知滴定反应为
5H2O2+2MnO4-+6H+=2Mn2++5O2+8H2O
将25.00mL AgNO3溶液和0.1293g NaCl反应,过量的AgNO3需用3.25mL NH4SCN溶液滴定。已知滴定20.00mL AgNO3溶液需要用21.00mLNH4SCN溶液。计算AgNO3和NH4SCN溶液的浓度。已知NaCl的相对分子质量为58.44。
配制c(1∕2H2SO4)=0.1000mol∕L硫酸溶液1000mL,需用质量分数为98﹪的浓硫酸(密度为ρ=1.84g∕cm3)()mL。
计算题:配制c(1∕2H2SO4)=0.1000mol∕L硫酸溶液1000mL,需用质量分数为98﹪的浓硫酸(密度为ρ=1.84g∕cm3)多少毫升?


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题