 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
氮的价电子层构型是2s22p3,试用四个量子数分别表明每个电子的运动状态。
氮的价电子层构型是2s22p3,试用四个量子数分别表明每个电子的运动状态。
提问人:网友anonymity
发布时间:2022-01-06
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
氮的价电子层构型是2s22p3,试用四个量子数分别表明每个电子的运动状态。
 更多“氮的价电子层构型是2s22p3,试用四个量子数分别表明每个电…”相关的问题
更多“氮的价电子层构型是2s22p3,试用四个量子数分别表明每个电…”相关的问题
价电子层构型为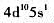 的元素,其原子序数为()
的元素,其原子序数为()
A.25
B.39
C.41
D.47
E.57
主族元素AB3型分子有三种几何构型,它们分别是______、______和______;每种构型中,中心原子A的价电子层孤对电子数为______、______和______。
完成下表(不看周期表):
原子序数 | 电子层结构 | 价层电子构型 | 区 | 周期 | 族 | 金属或非金属 |
[Ne]3s23p5 | ||||||
4d55s1 | ||||||
6 | ⅡB | |||||
88 |
设有元素A、B、C、D、E、G、M,试按下列所给的条件,推断它们的元素符号及在周期表中的位置(周期、族),并写出它们的价层电子构型。
(1) A、B、C为同一周期的金属元素,已知C有三个电子层,它们的原子半径在所属周期中为最大,并且A>B>C;
(2) D、E为非金属元素,与氢化合生成HD和HE,在室温时D的单质为液体,E的单质为固体;
(3) G是所有元素中电负性最大的元素;
(4) M为金属元素,它有四个电子层,它的最高氧化数与氯的最高氧化数相同。


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题