 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
反应SO2(g)+1/2O2(g)=SO2(g)的标准吉布斯自由能变与温度的关系为ΔrGmθ=(-94500+89.50T/K)Jmol-1.若反应起始时系统中含SO2为6%(摩尔分数,下同),含O2为12%,则在标准压力下,欲使SO2的中衡转化率达90%,反应温度应控制为若干?
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 更多“加氢裂化反应的反应温度与转化率的关系为线性关系,即反应温度升…”相关的问题
更多“加氢裂化反应的反应温度与转化率的关系为线性关系,即反应温度升…”相关的问题
反应SO2(g)+1/2O2(g)=SO2(g)的标准吉布斯自由能变与温度的关系为ΔrGmθ=(-94500+89.50T/K)Jmol-1.若反应起始时系统中含SO2为6%(摩尔分数,下同),含O2为12%,则在标准压力下,欲使SO2的中衡转化率达90%,反应温度应控制为若干?
与温度的关系为
k=3.452×10-5exp(-10983/T) [kmol/(s·kg·Pa)]
不同温度下的化学平衡常数值可根据下列近似式估算:
K=3.96×1011exp(-14.520/T) (Pa-1)
反应混合物的平均比热容为2.177kJ/(kg·K),反应热为1.39×105J/mol,催化剂床层的堆密度为1440kg/m3。试计算
(1)催化剂用量;
(2)反应器的轴向温度及转化率分布。
400K~500K间,理想气体反应PCI5(g)=PCl3(g)+Cl2(g)的标准反应摩尔吉布斯函数与温度的关系为: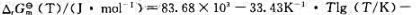
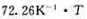
(1)计算
(2)往1.00dm3的容器中注人1.000gPCl5(g),于450.0K下达到平衡,计算PCl5(g)的平衡转化率和容器内的总压.P和Cl的摩尔质量分别为31.0g·mol-1和35.5g·mo-1.
(3)物质的量比值为1:5的PCl5(g)与CI2(g)的混合物,在450.0K,100kPa下,求达到化学平衡时PCl5(g)的平衡转化率.
(4)在上述已达平衛的容器中再通入He气,使容器内压力增大一倍,但温度和体积不变,这时PCl5(g)的平衡转化率有何变化?
已知反应 的
的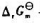 与T的关系为
与T的关系为
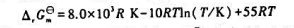
则此反应的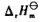 与T之间的函数关系为
与T之间的函数关系为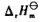 =();
=();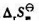 与T之间的函数关系为
与T之间的函数关系为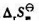 =();InKθ与T之间的函数关系为lnKθ=().若T=1000K,p=200kPa,则题给反应的标准平衡常数Kθ和B2(g)的平衡转化率α分别为Kθ=(),α=().
=();InKθ与T之间的函数关系为lnKθ=().若T=1000K,p=200kPa,则题给反应的标准平衡常数Kθ和B2(g)的平衡转化率α分别为Kθ=(),α=().
A.反应速度直接取决于反应温度
B. 加氢裂化反应器中催化剂床层总温升是转化率的标志
C. 原料性质不同,一般反应温度也不相同
D. 加氢裂化反应中,温度条件的选择原则是在力求催化剂活性允许的条件下,采用尽可能高的反应温度


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题