 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
某氧化还原反应组成原电池,测得电动势大于零,这意味着()
A.ΔrGmӨ>0 ; KӨ>1
B.ΔrGmӨ>0 ; KӨ<1<br>
C.ΔrGmӨ<0 ; kө>1
D.ΔrGmӨ<0 ;>
提问人:网友lost00
发布时间:2022-01-06
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.ΔrGmӨ>0 ; KӨ>1
B.ΔrGmӨ>0 ; KӨ<1<br>
C.ΔrGmӨ<0 ; kө>1
D.ΔrGmӨ<0 ;>
 更多“某氧化还原反应组成原电池,测得电动势大于零,这意味着()”相关的问题
更多“某氧化还原反应组成原电池,测得电动势大于零,这意味着()”相关的问题
将氧化还原反应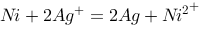 设计为一个原电池,已知
设计为一个原电池,已知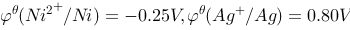 ,则原电池的电动势
,则原电池的电动势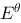 为1.05 (V),
为1.05 (V),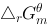 为-203 kJ/mol,该氧化还原反应的平衡常数为
为-203 kJ/mol,该氧化还原反应的平衡常数为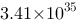 。
。
A、原电池正极发生还原反应,负极发生氧化反应
B、原电池中氧化剂在原电池的正极
C、原电池的电池反应就是作为氧化剂的物质同作为还原剂的物质起反应
D、原电池中,电极电位较低的电对组成电池的正极
由两个氢电极H2(100kPa)|H+(0.10mol·dm-3)|Pt和H2(100kPa)|H+(xmol·dm-3)|Pt组成原电池,测得该原电池的电动势为0.016V。若后一电极作为该原电池的正极,求组成该电极的溶液中H+的浓度x的值。
某氢电极与饱和甘汞电极(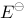 =+0.240 v)组成原电池 ,若要使电池电动势达到 +0.299 v ,则溶液的 pH 值是
=+0.240 v)组成原电池 ,若要使电池电动势达到 +0.299 v ,则溶液的 pH 值是
A、1
B、2
C、3
D、4
A、S2-<cl-<k+<ca2+<br> B、Cl-<s2-<k+<ca2+<br> C、K+<ca2+<cl-<s2-<br> D、Ca2+<k+<cl-<s2-<br>


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题