 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
25℃时,在Cu2+的氨水溶液中,平衡时![25℃时,在Cu2+的氨水溶液中,平衡时,并认为有50%的Cu2+形成了配离子[Cu(NH3)4]2](https://img2.soutiyun.com/latex/latex.action) ,并认为有50%的Cu2+形成了配离子[Cu(NH3)4]2+,余者以Cu2+形式存在。则[Cu(NH3)4]2+的不稳定常数为( )。
,并认为有50%的Cu2+形成了配离子[Cu(NH3)4]2+,余者以Cu2+形式存在。则[Cu(NH3)4]2+的不稳定常数为( )。
A.4.5×10-7
B.2.0×10-13
C.6.7×10-4
D.数据不足,无法确定
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
![25℃时,在Cu2+的氨水溶液中,平衡时,并认为有50%的Cu2+形成了配离子[Cu(NH3)4]2](https://img2.soutiyun.com/latex/latex.action) ,并认为有50%的Cu2+形成了配离子[Cu(NH3)4]2+,余者以Cu2+形式存在。则[Cu(NH3)4]2+的不稳定常数为( )。
,并认为有50%的Cu2+形成了配离子[Cu(NH3)4]2+,余者以Cu2+形式存在。则[Cu(NH3)4]2+的不稳定常数为( )。A.4.5×10-7
B.2.0×10-13
C.6.7×10-4
D.数据不足,无法确定
 更多“25℃时,在Cu2+的氨水溶液中,平衡时,并认为有50%的C…”相关的问题
更多“25℃时,在Cu2+的氨水溶液中,平衡时,并认为有50%的C…”相关的问题
往含有0.1mol/L的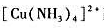 配离子溶液中,加入氨水,使溶液中NH3浓度为1.0mol/L,请计算达到平衡时溶液中Cu2+离子浓度为多少?已知
配离子溶液中,加入氨水,使溶液中NH3浓度为1.0mol/L,请计算达到平衡时溶液中Cu2+离子浓度为多少?已知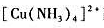 的
的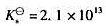
0.025mol·dm-3的Cu2+离子溶液10cm3与0.30mol·dm-3氨水10cm3混合,求溶液中Cu2+离子的平衡浓度。已知lgK稳(Cu(NH3)42+)=13.32。
A.Fe3+,Al3+被沉淀,而Cu2+,Zn2+,Ca2+,Mg2+在溶液中
B.Fe3+,Al3+,Ca2+,Mg2+被沉淀,而Cu2+,Zn2+在溶液中
C.Ca2+,Mg2+被沉淀,而Fe3+,Al3+,Cu2+,Zn2+在溶液中
D.Cu2+,Zn2+被沉淀,而Fe3+,Al3+,Ca2+,Mg2+在溶液中
25℃时,
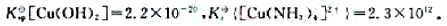 将10mL0.10mol·L-1CuSO6溶液与10mL6.0mol·L-1NH3溶液混合,计算平衡时溶液中Cu2+,NH3和[Cu(NH3)4]2+的浓度。如果向此混合溶液中加入0.010molNaOH固体,是否有Cu(OH)2沉淀生成?
将10mL0.10mol·L-1CuSO6溶液与10mL6.0mol·L-1NH3溶液混合,计算平衡时溶液中Cu2+,NH3和[Cu(NH3)4]2+的浓度。如果向此混合溶液中加入0.010molNaOH固体,是否有Cu(OH)2沉淀生成?
A.Li+、Na+、K+
B.Zn2+、Cd2+、Cu2+
C.Cu2+、Mg2+、Fe3+
D.Hg2+、Al3+、Mn2+
查得总压为101.3kPa,温度为25℃时,在100g水中含氨1g,该溶液上方蒸汽的平衡分压p*为0.986kPa。已知在此浓度范围内,该溶液服从亨利定律,稀氨水溶液的密度可按纯水计算。试求溶解度系数H[以kmol/(m3·kPa)为单位]和相平衡系数m。
25℃时,Cu元素在酸性溶液中的元素标准电极电势图为
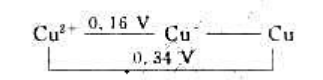
(1)试计算25℃时电对Cu2+/Cu的标准电极电势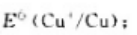
(2)已知2.303RT/F=0.060V,试计算25℃时Cu2+的歧化反应的标准平衡常数,
在25℃时用标准加入法测定Cu2+浓度,于100mL铜盐溶液中添加0.1mol·L-1Cu(NO3)2溶液1.0mL时,电动势增加10mV。求原溶液的总离子浓度。(设电极系数符合理论值)
A.Fe3+、Al3+、Mg2+被沉淀而Cu2+、Zn2+、Ca2+存在于溶液中
B.Fe3+、Al3+被定量沉淀,其余四种离子留在溶液中
C.六种离子均被沉淀
D.由于Al3+具有两性,故只有Fe(OH)3沉淀生成
E.Fe3+、Al3+、Cu2+、Zn2+形成沉淀,Ca2+、Mg2+留于溶液中


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题