 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
欲配制草酸钠溶液以标定0.04000mol·L-1KMnO4溶液,如果使标定时两种溶液消耗的体积相等,则草酸钠应配制的浓
欲配制草酸钠溶液以标定0.04000mol·L-1KMnO4溶液,如果使标定时两种溶液消耗的体积相等,则草酸钠应配制的浓度是多少?
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
欲配制草酸钠溶液以标定0.04000mol·L-1KMnO4溶液,如果使标定时两种溶液消耗的体积相等,则草酸钠应配制的浓度是多少?
 更多“欲配制草酸钠溶液以标定0.04000mol·L-1KMnO4…”相关的问题
更多“欲配制草酸钠溶液以标定0.04000mol·L-1KMnO4…”相关的问题
用草酸钠溶液标定浓度为0.04000 mol/L的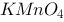 溶液,如果使标定时所消耗草酸钠溶液体积和
溶液,如果使标定时所消耗草酸钠溶液体积和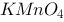 溶液体积相等,则草酸钠的浓度应为( )
溶液体积相等,则草酸钠的浓度应为( )
A、0.1000 mol/L
B、0.04000 mol/L
C、0.05000 mol/L
D、0.08000 mol/L
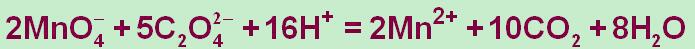
A、0.1000
B、0.041000
C、0.05000
D、0.08000
A、2MnO4-+5C2O42-+8H+==2Mn2++10CO2↑+4H2O
B、温度75~85℃
C、酸度 0.5~1.0mol/L,硫酸介质;
D、滴定速度:为自动催化反应,褪色后再加第二滴,
A、用电子天平称取2.00 g NaOH固体,在烧杯中溶解后,转移到500 mL试剂瓶中,稀释到刻度
B、用电子分析天平称取2.0000 g NaOH固体,在烧杯中溶解后,转移到500 mL容量瓶中,稀释到刻度
C、用电子天平称取2.00 g NaOH固体,在烧杯中溶解后,转移到500 mL容量瓶中,稀释到刻度
D、用电子分析天平称取2.0000 g NaOH固体,在烧杯中溶解后,转移到500 mL试剂瓶中,稀释到刻度
某基准物质A的摩尔质量为130g·mol-1,用A标定0.02mol·L-1的B溶液,如滴定管读数可估计到±0.01mL,要求的滴定误差小于0.1%,标定反应为5A+2B=2P,,问基准物A的称取量至少应为多少克?
用基准物Na2CO3标定HCl溶液时,下列情况会对HCl的浓度产生何种影响:A正误差;B负误差;C无影响;D结果混乱。
①滴定时速度太快,附在滴定管壁的HCl来不及流下来就读取滴定剂体积。
②称取Na2CO3时,实际质量为0.1834g,记录时误记为0.1824g。
③锥瓶中的Na2CO3用蒸馏水溶解时,多加了50mL蒸馏水。
④滴定开始之前,忘记调节零点,HCl溶液的液面高于零点。
⑤称取Na2CO3时,撒在天平盘上。
⑥配制HCl溶液时没有混匀。
NaOH标准溶液因保存不当吸收了CO2,若以此NaOH溶液滴定H3PO4至第二个计量点,则H3PO4的分析结果将偏高、偏低或无影响?
A.50 Ml
B.250 mL
C.100 mL
D.500 mL


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题