 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某系统存在C(s)、H2O(g)、CO(g)、CO2(g)和H2(g)五种物质,并建立了下述平衡: H2O(g) + C(s) = H2(g) + CO(g)、CO2(g) + H2(g) = H2O(g) + CO(g)、CO2(g) + C(s) = 2 CO(g)则该系统的组分数K为
A.3
B. 2
C. 1
D. 4
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.3
B. 2
C. 1
D. 4
 更多“某系统存在C(s)、H2O(g)、CO(g)、CO2(g)和…”相关的问题
更多“某系统存在C(s)、H2O(g)、CO(g)、CO2(g)和…”相关的问题
:①Ni0(s)+C0(g) Ni(s)+CO2(g);②H2O(l)+CO(g)
Ni(s)+CO2(g);②H2O(l)+CO(g) H2(g)+CO2(g);③NiO(s)+H2(g)
H2(g)+CO2(g);③NiO(s)+H2(g)
Ni(s)+H2O(l),该系统的S=(),C=(),f=().
A.C=3;
B.C=2;
C.C=1;
D.C=4
某体系存在C(s),H2O(g),CO(g),CO2(g),H2(g)五种物质,相互建立了下述三个平衡:
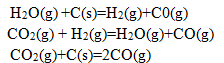
则该体系的独立组分数C为()。
A.C=3
B.C=2
C.C=1
D.C=4
如果系统中有下列相存在,而且在给定的物质之问建立了化学平衡,试确定系统的组分数.
(1)HgO(s)、Hg(g)、O2(g);
(2)C(8)、H2O(g)、H2(g)、CO(g)、CO2(g);
(3)Fe(s)、FeO(s),CO
(4)Fe(s)、FeO(s)、C(s)、CO(g)、CO2(g).
在制水煤气的过程中,有五种物质C(s)、CO(g)、CO2(g)、H2(g)和H2O(g)建立如下三个平衡。试求系统的独立组分数。
C(s)+H2O(g)===H2(g)+CO(g) ①
CO2(g)+H2(g)===H2O(g)+CO(g) ②
CO2(g)+C(s)===2CO(g) ③
对反应系统C(s)+H2O(g)====CO(g)+H2(g),由于化学方程式两边物质的化学计量数的总和相等,所以增加总压力对平衡无影响。
炉中共有C(s)、H2(g)、H2O(g)、CO(g)和CO2(g)五种物质,其间可能相互发生反应。试求该系统的组分数C。
A.平衡时系统压力为100kPa
B.增大压力不影响此反应的平衡移动
C.此反应的定容热Qv=133.9KJ?mol-1
D.升高温度将提高碳的转化率
煤和由煤与水蒸气反应[C(s)+H2O(g)=H2(g)+CO(g)]而得的水煤气(CO与H2等物质的混合物)都可用做燃料。设煤含碳80%,其余可燃成分忽略不计。试通过计算说明,在实际应用中以水煤气代替煤作燃料的优点。(提示:在任何能量转换过程中,总会有一些能量变成热而扩散到环境中。例如,欲往某体系输入xkJ的能量,实际上提供的热量要远多于该值。)


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题