 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
理想气体反应N2O5(g)===N2O4(g)+(1/2)O2(g)的 为41.84kJ·mol-1,△Cp,m=0。要增加N2O4的产率可以:( )。
为41.84kJ·mol-1,△Cp,m=0。要增加N2O4的产率可以:( )。
A.降低温度
B.提高温度
C.提高压力
D.等温等容加入惰性气体
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 为41.84kJ·mol-1,△Cp,m=0。要增加N2O4的产率可以:( )。
为41.84kJ·mol-1,△Cp,m=0。要增加N2O4的产率可以:( )。A.降低温度
B.提高温度
C.提高压力
D.等温等容加入惰性气体
 更多“理想气体反应N2O5(g)===N2O4(g)+(1/2)O…”相关的问题
更多“理想气体反应N2O5(g)===N2O4(g)+(1/2)O…”相关的问题
A、125 kPa
B、75.0 kPa
C、7.500 kPa
D、25 kPa
A、2´106 Pa×m3
B、106 Pa×m3
C、105 Pa×m3
D、0
已知445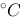 时,
时,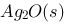 的分解压力为20974kPa,则此时分解反应
的分解压力为20974kPa,则此时分解反应 的
的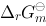 为 ( )
为 ( )
A、-15.92kJ/mol
B、14.38kJ/mol
C、15.92kJ/mol
D、-31.83kJ/mol
已知 445℃时,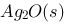 的分解压力为20 974 kPa,则此时分解反应
的分解压力为20 974 kPa,则此时分解反应 的
的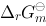 为:
为:
A、-15.92 kJ/mol
B、14.387 J/mol
C、15.92 kJ/mol
D、-31.83 kJ/mol
理想气体反应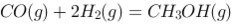 的
的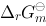 与温度T 的关系为: \Delta _rG_m^ \ominus
与温度T 的关系为: \Delta _rG_m^ \ominus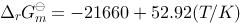 (in J/mol),若要使反应的平衡常数
(in J/mol),若要使反应的平衡常数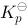 >1,则应控制的反应温度( )
>1,则应控制的反应温度( )
A、必须低于409.3K
B、必须低于409.3℃
C、必须等于409.3K
D、必须高于409.3K
A、降低温度, 升高压力
B、升高温度, 降低压力
C、降低温度, 降低压力
D、升高温度, 升高压力
反应 在101 325 Pa、分解温度时的分压
在101 325 Pa、分解温度时的分压 等于: ( )
等于: ( )
A、(2/3)×101.325 kPa
B、101.325 kPa
C、(101.325 /2) kPa
D、(101.325 /3) kPa
已知分解反应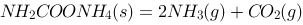 在30℃时的平衡常数K=0.000655,则此时
在30℃时的平衡常数K=0.000655,则此时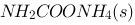 的分解压力为:( )
的分解压力为:( )
A、16630Pa
B、594000Pa
C、5542Pa
D、2928Pa


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题