 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
把HCOOH、HAc、H3PO4、HCOONa、NaAc、NaH2PO4几种溶液中的哪两种溶液相混合,可以配制成pH=3.50的缓冲
 参考答案
参考答案
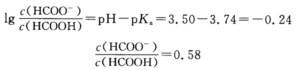 取1.00 dm30.100mol.dm-3HCOOH溶液(含HCOOH 0.100mol)和0.58 dm30.100mol.dm-3HCOONa溶液(含HCOONa 0.058 mol)相混合即得。
取1.00 dm30.100mol.dm-3HCOOH溶液(含HCOOH 0.100mol)和0.58 dm30.100mol.dm-3HCOONa溶液(含HCOONa 0.058 mol)相混合即得。有关的pK如下:选用HCOOH-HCOONa溶液为好,其pK=3.7,接近所需配缓冲溶液的pH(3.50)。取1.00dm30.100mol.dm-3HCOOH溶液(含HCOOH0.100mol)和0.58dm30.100mol.dm-3HCOONa溶液(含HCOONa0.058mol)相混合,即得。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案


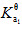 (H3PO4)=2.12;欲配制pH=3.5的缓冲溶液500mL,并使溶液中酸的浓度为0.20mol•L-1。应选用哪种缓冲对?需称取多少固体钠盐?
(H3PO4)=2.12;欲配制pH=3.5的缓冲溶液500mL,并使溶液中酸的浓度为0.20mol•L-1。应选用哪种缓冲对?需称取多少固体钠盐?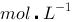 )H3PO4 + c2 (
)H3PO4 + c2 (

















