 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
计算题2:H2和N2的混合气体40.00mL,加空气经燃烧后,测得其总体积减少18.00mL,求H2在混合气体中的体积分数。
提问人:网友royone
发布时间:2022-01-07
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 更多“计算题2:H2和N2的混合气体40.00mL,加空气经燃烧后…”相关的问题
更多“计算题2:H2和N2的混合气体40.00mL,加空气经燃烧后…”相关的问题
有一混合气体,总压为150Pa,其中N2和H2的体积分数分别为0.25和0.75,求H2和N2的分压。
A、10%
B、40%
C、50%
D、90%
由C2H4和过量H2组成的混合气体的总压为6930Pa。使混合气体通过铂催化剂进行下列反应:
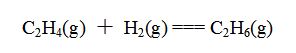
待完全反应后,在相同温度和体积下,压强降为4530Pa。求原混合气体中C2H4的物质的量分数。
已知在25℃及101kPa压力下,含有N2和H2的混合气体的密度为0.50g·dm-3,则N2和H2的分压及体积分数各是多少?
厌氧培养箱工作时,箱体内气体是
A.O2、H2、CO2混合气体
B.N2、H2、CO2混合气体
C.O2、CO2、N2混合气体
D.CO2、H2混合气体
E.CO2、H2混合气体
(1)保持容器内温度恒定抽去隔板,计算气体混合后的压力;
(2)分别计算混合气体中H2和 N2的分压;
(3)分别计算混合气体中H2和N2的分体积.


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题