 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
改变氧化还原反应中某反应物的浓度就很容易使反应方向逆转,是那些标准电动势接近零的反应。
提问人:网友laishenglei
发布时间:2022-01-07
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 更多“改变氧化还原反应中某反应物的浓度就很容易使反应方向逆转,是那…”相关的问题
更多“改变氧化还原反应中某反应物的浓度就很容易使反应方向逆转,是那…”相关的问题
A.氧化还原反应达到平衡时平衡常数K为零
B.氧化还原反应达到平衡时标准电动势E为零
C.负极发生还原反应,正极发生氧化反应
D.负极是还原态物质失电子,正极是氧化态物质得电子
某氧化还原反应组装成原电池,下列说法正确的是
(A) 负极发生还原反应,正极发生氧化反应
(B) 负极是还原态物质失电子,正极是氧化态物质得电子
(C) 氧化还原反应达平衡时平衡常数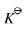 为零
为零
(D) 氧化还原反应达平衡时标准电动势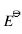 为零
为零
A.电池电动势大于零
B.电池电动势小于零
C.标准电池电动势大于零
D.标准电池电动势小于零
E.标准电池电动势等于零


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题