 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
已知下列电池在25℃时的电动势为-0. 52V,求算aH+和该电极的pH。 (—)Pt|H2(100kPa)|H+(1.0mol·L-1)||H+(aH+)|
已知下列电池在25℃时的电动势为-0. 52V,求算aH+和该电极的pH。
(—)Pt|H2(100kPa)|H+(1.0mol·L-1)||H+(aH+)|H2(100kPa)|Pt()
提问人:网友anonymity
发布时间:2022-01-06
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知下列电池在25℃时的电动势为-0. 52V,求算aH+和该电极的pH。
(—)Pt|H2(100kPa)|H+(1.0mol·L-1)||H+(aH+)|H2(100kPa)|Pt()
 更多“已知下列电池在25℃时的电动势为-0. 52V,求算aH+和…”相关的问题
更多“已知下列电池在25℃时的电动势为-0. 52V,求算aH+和…”相关的问题
A、羟氨(NH2OH) Kby = 1.0×10-9
B、亚硝酸Kay = 5.1×10-4
C、醋酸Kay = 1.8×10-5
D、氨水Kby = 1.8×10-5
pH玻璃电极|H+(a=x)‖饱和甘汞电极
当分别用三种未知溶液代替标准缓冲溶液时,测得电动势为:①0.312V;②0.088V;③-0.017V。试计算每种溶液的pH及氢离子活度。
A、219.2
B、109.6
C、-219.2
D、-109.6
25℃,101 325 Pa的液态H2O的化学势为 (l),25℃,101 325 Pa的气态H2O的化学势为
(l),25℃,101 325 Pa的气态H2O的化学势为 (g) ,二者的关系是( )
(g) ,二者的关系是( )
A、 (l) >
(l) > (g)
(g)
B、 (l) <
(l) < (g)
(g)
C、 (l) =
(l) = (g)
(g)
D、无法判断
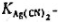 。(已知
。(已知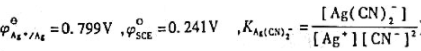 )
)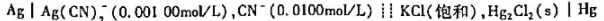
自发电池HgHg2Cl2(s),Cl-(饱和)〡Mn+〡M。在25℃时,测得电动势为0.100V,如将Mn+浓度稀释50倍,电池电动势下降为0.050V,金属离子Mn+的电荷n为何值?
已知下列电池在25℃时的电动势为0.125V,求算cCu2+。
(—)Cu|Cu2+(1.0×10-4mol·L-1)||Cu2+(c)|Cu()


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题