 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
对反应PCl3(g)+Cl2(g)====PCl5(g),如何能提高PCl3的转化率。( )
A.增加PCl5的压力
B.减小总压
C.加入催化剂
D.增加Cl2的压力
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.增加PCl5的压力
B.减小总压
C.加入催化剂
D.增加Cl2的压力
 更多“对反应PCl3(g)+Cl2(g)====PCl5(g),如…”相关的问题
更多“对反应PCl3(g)+Cl2(g)====PCl5(g),如…”相关的问题
A. 130.38kPa
B. 0.767kPa
C. 7607kPa
D. 7.67×10-3kPa
可逆反应PCl5(g)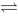 PCl3(g)+Cl2(g)在密闭容器中进行,其焓变小于零。当达到平衡时,下列说法正确的是
PCl3(g)+Cl2(g)在密闭容器中进行,其焓变小于零。当达到平衡时,下列说法正确的是
A、平衡条件不变,加入催化剂使平衡向右移动
B、保持体积不变,加入氮气使压力增加1倍,平衡向左移动
C、保持压力不变,通入氯气使压力增加1倍,平衡向左移动
D、向体系通入惰性气体,或降低温度,平衡向右移动
在一定温度下,反应PCl3(g)+Cl2(g)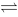 PCl5(g)达到平衡,当进行下列操作时,平衡不发生变化的是
PCl5(g)达到平衡,当进行下列操作时,平衡不发生变化的是
A、在恒容条件下,通入一定量的水蒸气
B、在恒容条件下,通入一定量的氮气
C、在恒压条件下,通入一定量的氮气
D、在恒压条件下,通入一定量的水蒸气
(1) HAc;(2) NaAc;(3) NH3;(4) H2SO4;(5) NH4Cl;(6) NH4Ac。
某溶液含有Mn2+,Pb2+,它们的浓度均为0.10mol·dm-3。在室温下通入H2S使其成为H2S饱和溶液,并加HCl控制S2-浓度。为了使PbS沉淀出来,而Mn2+仍然留在溶液中,则溶液中的H+浓度最低应是多少?此时溶液中的Pb2+浓度是否小于1×10-5mol·dm-3?
某溶液含有Ag+,Pb2+,Sr2+,各离子浓度均为0.100mol·dm-3。如果慢慢滴加K2CrO4溶液,溶液体积变化忽略不计。通过计算说明上述离子的铬酸盐开始沉淀的顺序。
0.020dm3,0.60mol·dm-3氨水和0.010dm3,1.80mol·dm-3NH4Cl溶液混合,溶液的pH为多少?若加入0.001dm3,0.1mol·dm-3的HCl溶液,pH变为多少?
A.1mol·dm-3NaCl溶液 B.1mol·dm-3AgNO3溶液
C.H2O D.2mol·dm-3NaNO3溶液


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题