 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
分别计算反应Ni(s)+Sn2+(aq)=Ni2+(aq)+Sn(s)(假设离子浓度均为1mol•dm-3):
(1)它们组成原电池的电动势,并指出正负极。
(2)25℃时的标准平衡常数。
(3)反应的标准吉布斯函数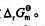
分析:本题主要考查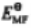 与
与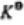 和
和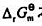 之间的换算关系。由于已经假设是在标准状下,所以不需要计算电极电势。
之间的换算关系。由于已经假设是在标准状下,所以不需要计算电极电势。
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
(1)它们组成原电池的电动势,并指出正负极。
(2)25℃时的标准平衡常数。
(3)反应的标准吉布斯函数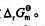
分析:本题主要考查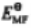 与
与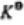 和
和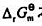 之间的换算关系。由于已经假设是在标准状下,所以不需要计算电极电势。
之间的换算关系。由于已经假设是在标准状下,所以不需要计算电极电势。
 更多“分别计算反应Ni(s)+Sn2+(aq)=Ni2+(aq)+…”相关的问题
更多“分别计算反应Ni(s)+Sn2+(aq)=Ni2+(aq)+…”相关的问题
根据下列反应(假设离子浓度均为1.0molL-1) Ni(s)+Sn2+(aq)=Ni2+(aq)+Sn(s) Cl2(g)+2Br-1(aq)=Br2(l)+2Cl-(aq) 试分别计算: (1)它们组成的原电池电动势,并指出正负极。 (2)298K时的平衡常数。 (3)298K反应的标准吉布斯函数变△rGΘm。
反应2NO2(g)→N2O4(g),假设NO2(g),N2O4(g)均为理想气体。在298.15K该反应分别按以下两种途径完成:(1)不做功、放热57.2kJ·mol-1;(2)做功、放热11.3kJ·mol-1。计算两种途径的Q,W,△U和△H。
若有关金属离子的浓度均为0.01mol·L-1,计算说明在pH=4.5时,Fe2+,Mg2+,Zn2+,Ca2+各离子能否被单独滴定?
分别计算浓度为0.1mol/kg的CuSO4(γ±=0.164)和K4Fe(CN)6(γ±=0.141)的离子平均质量摩尔浓度、离子平均活度以及电解质的活度。
将液Br2加入到Cl-离子的水溶液中,在Cl2气压强为100kPa时,反应达平衡,试计算Cl-离子和Br-离子的浓度比。
某溶液含有Ag+、Pb2+、Ba2+等离子,其浓度均为0.1mol/L,通过计算说明滴加K2CrO4溶液时上述离子开始沉淀的顺序。
某溶液含Mg2+和Ca2+离子,浓度均为0.5 0 mol.dm-3,计算说明滴加(NH4)2C2O4溶液时,哪种离子先沉淀?当第一种离子沉淀完全时(即残留浓度≤1.0×1 0-5 mol.dm-3),第二种离子沉淀了百分之几? (CaC2O4的Kspθ=2.6×10-9,MgC2O4的Kspθ=8.5×10-5)
某溶液含有Ag+,Pb2+,Sr2+,各离子浓度均为0.100mol·dm-3。如果慢慢滴加K2CrO4溶液,溶液体积变化忽略不计。通过计算说明上述离子的铬酸盐开始沉淀的顺序。


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题