 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
对于下列平衡体系:C(s)+H2O(g)====CO(g)+H2(g),Q为正值。
对于下列平衡体系:C(s)+H2O(g)====CO(g)+H2(g),Q为正值。
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
对于下列平衡体系:C(s)+H2O(g)====CO(g)+H2(g),Q为正值。
 更多“对于下列平衡体系:C(s)+H2O(g)====CO(g)+…”相关的问题
更多“对于下列平衡体系:C(s)+H2O(g)====CO(g)+…”相关的问题
A、达平衡时p(H2O)=p(CO)=p(H2),即反应物与生成物压力相等
B、达平衡后p(H2O)、p(CO)、p(H2)不再改变
C、由于反应前后分子数不变,所以增加压力对平衡没有影响
D、升高温度,平衡逆向移动
某温度时,下列反应已达平衡:CO(g)+H2O(g)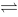 CO2(g)+H2(g) ΔrHmө = -41.2kJ·mol-1,为提高CO转化率可采用
CO2(g)+H2(g) ΔrHmө = -41.2kJ·mol-1,为提高CO转化率可采用
A、A、压缩容器体积,增加总压力
B、B、扩大容器体积,减少总压力
C、C、升高温度
D、D、降低温度
某体系存在C(s),H2O(g),CO(g),CO2(g),H2(g)五种物质,相互建立了下述三个平衡:
H2O(g)+C(s)====H2(g)+CO(g)
CO2(g)+H2(g)====H2O(g)+CO(g)
CO2(g)+C(s)====2CO(g)
则该体系的独立组分数C为( )。
A.C=3; B.C=2; C.C=1; D.C=4
一级反应A→B+C,已知A的起始浓度为0.50mol·dm-3,速率常数k=5.3×10-3s-1,试求:这个反应的速率
零级反应A→B+C,已知A的起始浓度为0.36mol·dm-3,完全分解用了1.0h,试求该反应以s-1为单位表示的速率常数。
某反应A→B,当反应物A的浓度c(A)=0.200mol·dm-3时,反应速率为0.005mol·dm-3·s-1。试计算在下列情况下,反应速率常数各为多少?
根据实验,NO和Cl2的反应
2NO(g)+Cl2(g)→2NOCl(g)
满足质量作用定律。
(A) 4倍 (B) 2倍 (C) 8倍
(D) 1/8倍 (E) 1/4倍


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题