 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


若 298K 时反应N2O4 (g) = 2NO2(g) 的 Kө =0.1132,则当 N2O4 和 NO2 的分压均为1.0 kPa 时,
若 298K 时反应N2O4 (g) = 2NO2(g) 的 Kө =0.1132,则当 N2O4 和 NO2 的分压均为1.0 kPa 时, 该反应()
A向生成 NO2 的方向进行
B向生成 N2O4 的方向进行
C正好达到化学平衡
D难于判断其进行方向
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


若 298K 时反应N2O4 (g) = 2NO2(g) 的 Kө =0.1132,则当 N2O4 和 NO2 的分压均为1.0 kPa 时, 该反应()
A向生成 NO2 的方向进行
B向生成 N2O4 的方向进行
C正好达到化学平衡
D难于判断其进行方向
 更多“若 298K 时反应N2O4 (g) = 2NO2(g) 的…”相关的问题
更多“若 298K 时反应N2O4 (g) = 2NO2(g) 的…”相关的问题
A.已达平衡
B.逆向进行
C.正向进行
D.无
A.向生成NO2的方向进行
B. 正好达到平衡
C. 难以判断其进行的方向
D. 向生成N2O4的方向进行
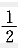 O2(g)=H2O(L),△H=-285.8kJ/mol。若温度升高,则有下列中何种变化?()
O2(g)=H2O(L),△H=-285.8kJ/mol。若温度升高,则有下列中何种变化?()
A.正反应速率增大,逆反应速率减小
B. 正反应速率增大,逆反应速率增大
C. 正反应速率减小,逆反应速率增大
D. 正反应速率减小,逆反应速率减小
A.正向自发
B.逆向自发
C.处于平衡态
D.不能确定
A.正向自发
B. 逆向自发
C. 处于平衡态
D. 不能确定
A.正反应速率增大,逆反应速率减小
B. 正、逆反应速率均增大
C. 正反应速率减小,逆反应速率增大
D. 正、逆反应速率均减小
某基元反应A(g)+B(g)→P(g),设在298K时的速率常数kp(298K)=2.777×10-5Pa-1·s-1;308K时,kp(308K)=5.55×10-5Pa-1·s-1。若A(g)和B(g)的原子半径和摩尔质量分别为rA=0.36nm,rB=0.41nm,MA=28g·mol-1,MB=71g·mol-1。试求在298K时,
1)
该反应的概率因子
P
;
(2)
反应的活化焓
△
r
*
H
m
,活化熵
△
r
*
S
m
和活化
Gibbs
自由能
△
r
*
G
m
。

A.处于平衡状态
B.逆向进行
C.正向进行
D.无法判断
已知反应在298K的热力学数据如下:CO2(g)+H2=====CO(g)+H2O(g)
2010040 已知反应在298K的热力学数据如下:
CO2(g)+H2=====CO(g)+H2O(g)
ΔfH (kJ·mol-1) -393.5 0 -110.5 -241.8
求:
(1)298K时的反应的焓变;
(2)若此系统在400K时各组分气体的分压为p(CO)=p(H2O)=125kPa,p(CO2)=p(H2)=25kPa,通过计算判断反应进行的方向.已知298K时的平衡常数K=1.25


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题