 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某分解反应在10℃的速率常数为4.5×10-3s-1,活化能为58kJ·mol-1,求在什么温度下,该反应的速率常数为10×10-4s-
某分解反应在10℃的速率常数为4.5×10-3s-1,活化能为58kJ·mol-1,求在什么温度下,该反应的速率常数为10×10-4s-1?
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某分解反应在10℃的速率常数为4.5×10-3s-1,活化能为58kJ·mol-1,求在什么温度下,该反应的速率常数为10×10-4s-1?
 更多“某分解反应在10℃的速率常数为4.5×10-3s-1,活化能…”相关的问题
更多“某分解反应在10℃的速率常数为4.5×10-3s-1,活化能…”相关的问题
A、0~300 K
B、300~1000 K
C、1000~10000 K
D、大于10000K
已知分解反应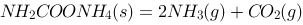 在30℃时的平衡常数K=0.000655,则此时
在30℃时的平衡常数K=0.000655,则此时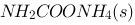 的分解压力为:( )
的分解压力为:( )
A、16630Pa
B、594000Pa
C、5542Pa
D、2928Pa
某药物按一级反应分解,反应速度常数K=5.27×10-5(h-1),则t0.9约为()
A. 2000h
B. 1000h
C. 200h
D. 100h
E. 20h
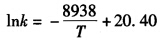 k的单位是h-1,T用绝对温标。求:(1)30℃时每小时分解百分之几?(2)若此药物分解30%即失效,30℃下保存的有效期为多长?(3)若要求此药物有效期达到2年,保存温度不能超过多少度?
k的单位是h-1,T用绝对温标。求:(1)30℃时每小时分解百分之几?(2)若此药物分解30%即失效,30℃下保存的有效期为多长?(3)若要求此药物有效期达到2年,保存温度不能超过多少度?
①2N2O5(g)→4NO2(g)+O2(g) Ea=103.3mol·L-1
②C2H5Cl(g)→C2H4(g)+HCl(g) Ea=246.9mol·L-1
(1)如果将反应温度由300K上升到310K,上述两反应的反应速率各增大多少倍?说明什么?
(2)如果将反应②的温度由700K上升到710K,反应的速率又增大多少倍?与②反应在(1)中的结果比较说明了什么?
N2+3H2=2NH3
在一定条件下,2.0mol·L-1的氮气与3.0mol·L-1的氢气反应,2秒末测得氨的浓度为0.4mol·L-1。分别计算氮气、氢气的消耗速率和氨的生成速率及整个反应的反应速率。


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题