 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
已知水的Kf=1.86 K.kg.mol-1,要使水溶液的凝固点降低1.00℃,需向200 g水中加入CaCl2的物质的量是
()
A.1.08 mol
B.0.108 mol
C.0.0540 mol
D.0.035 8 mol
提问人:网友funtsou
发布时间:2022-01-07
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.1.08 mol
B.0.108 mol
C.0.0540 mol
D.0.035 8 mol
 更多“已知水的Kf=1.86 K.kg.mol-1,要使水溶液的凝…”相关的问题
更多“已知水的Kf=1.86 K.kg.mol-1,要使水溶液的凝…”相关的问题
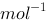
A、1.08mol
B、0.108mol
C、0.0540mol
D、0.0358mol
A、0.018 mol
B、0.054 mol
C、0.54 mol
D、0.027 mol
A. 99.8
B. 125
C. 209
D. 989
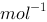 )是
)是
A、100
B、83.2
C、186
D、204
A、1.17%葡萄糖溶液
B、1.17%蔗糖溶液
C、0.20mol·dm-3葡萄糖溶液
D、0.40mol·dm-3蔗糖溶液
0.100mol·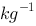 KCl溶液在稍高于-0.372℃时结冰,对这个现象的解释是(水的Kf=1.86K·kg·
KCl溶液在稍高于-0.372℃时结冰,对这个现象的解释是(水的Kf=1.86K·kg·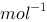 )
)
A、KCl未完全缔合
B、离子互吸
C、离子互斥
D、溶液蒸气压下降
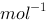 )
)
A、0.0100mol·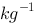
B、0.0200mol·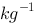
C、0.0346mol·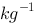
D、0.0372mol·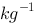
0.100mol·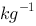 HAc溶液的电离度为1.33%,则该溶液的凝固点应为(水的Kf=1.86K·kg·
HAc溶液的电离度为1.33%,则该溶液的凝固点应为(水的Kf=1.86K·kg·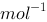 )
)
A、-0.25℃
B、-0.21℃
C、-0.188℃
D、-0.186℃


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题