 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[图]A、标准状态下自发变化的方向B、[图]C、在标准状态下...

A、标准状态下自发变化的方向
B、
C、在标准状态下系统所能作的最大非膨胀功
D、提高温度反应速率的变化趋势
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)

A、标准状态下自发变化的方向
B、
C、在标准状态下系统所能作的最大非膨胀功
D、提高温度反应速率的变化趋势
 更多“[图]A、标准状态下自发变化的方向B、[图]C、在标准状态下…”相关的问题
更多“[图]A、标准状态下自发变化的方向B、[图]C、在标准状态下…”相关的问题
A.标准状态下自发变化的方向
B.在ΔrG所对应的温度下的平衡位置
C.在标准状态下体系所能作的最大非膨胀功
D.提高温度反应速率的变化趋势
根据某一反应的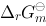 值,下列何者不能确定()
值,下列何者不能确定()
A、提高温度时反应速率的变化趋势
B、标准状态下自发变化的方向
C、在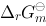 所对应的温度下的平衡位置
所对应的温度下的平衡位置
D、在标准状态下系统所能做的最大非体积功
根据某一反应的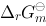 值,下列何者不能确定()
值,下列何者不能确定()
A、提高温度时反应速率的变化趋势
B、标准状态下自发变化的方向
C、在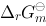 所对应的温度下的平衡位置
所对应的温度下的平衡位置
D、在标准状态下系统所能做的最大非体积功
判断在标准状态下反应N2(g) + O2(g) = 2NO (g)自发进行的方向,并解释之。已知平衡常数ΔrGm=298.15K。
根据某一反应的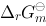 值,下列何者不能确定()
值,下列何者不能确定()
A、提高温度时反应速率的变化趋势
B、标准状态下自发变化的方向
C、在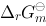 所对应的温度下的平衡位置
所对应的温度下的平衡位置
D、在标准状态下系统所能做的最大非体积功
300K、标准状态下,化学反应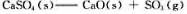 的标准摩尔焓变
的标准摩尔焓变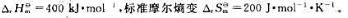
(1)在300K、标准状态下,上述反应能否自发进行?
(2)计算在标准状态下使上述反应自发进行的最低温度。
已知298.15K时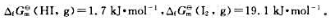 则化学反应
则化学反应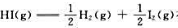 在298.15K时标准摩尔吉布斯自由能变
在298.15K时标准摩尔吉布斯自由能变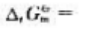 (),在标准状态下反应向方向自发进行。
(),在标准状态下反应向方向自发进行。
 ]
]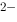 +4H
+4H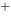 = 4HCN + Cu
= 4HCN + Cu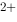 自发进行的方向应为()。(已知298.15K时,
自发进行的方向应为()。(已知298.15K时, {[Cu(CN)
{[Cu(CN)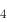 ]
]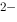 }=2.0×10
}=2.0×10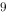 ,
, (HCN)=6.17×10
(HCN)=6.17×10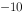 )
)
A.正向
B.逆向
C.平衡
D.三种情况都有可能


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题