 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用反应Zn^+2Ag^+⇌2Ag^+Zn^2+组成原电池,当[Zn^2+]和[Ag^+]均为1mol·dm^-3,在298.15K时,该电池的标准电动势E^θ池为()。
A.E^θ池=2E^θ(Ag^+/Ag)–E^θ(Zn^2+/Zn)
B.E^θ池=E^θ(Ag^+/Ag)]^2–E^θ(Zn^2+/Zn)
C.E^θ池=E^θ(Ag^+/Ag)–E^θ(Zn^2+/Zn)
D.E^θ池=E^θ(Zn^2+/Zn)–E^θ(Ag^+/Ag)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.E^θ池=2E^θ(Ag^+/Ag)–E^θ(Zn^2+/Zn)
B.E^θ池=E^θ(Ag^+/Ag)]^2–E^θ(Zn^2+/Zn)
C.E^θ池=E^θ(Ag^+/Ag)–E^θ(Zn^2+/Zn)
D.E^θ池=E^θ(Zn^2+/Zn)–E^θ(Ag^+/Ag)
 更多“用反应Zn^+2Ag^+⇌2Ag^+Zn^2+组成原电池,当…”相关的问题
更多“用反应Zn^+2Ag^+⇌2Ag^+Zn^2+组成原电池,当…”相关的问题
A、φ1-φ2
B、φ2-φ1
C、2φ1-φ2
D、φ1 -2φ2
A、增加0.0592V
B、降低0.0592V
C、降低0.0296V
D、增加0.0296V
A、变大
B、变小
C、不变
D、无法判断
A、0.059 V
B、-0.059 V
C、-0.118 V
D、0.118 V
原电池Zn + 2Ag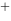 = Zn
= Zn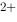 + 2Ag处于标准状态的电池电动势为( )。
+ 2Ag处于标准状态的电池电动势为( )。
A、ε= 2φ
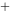 /Ag) - φ
/Ag) - φ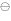 (Zn
(Zn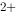 /Zn)
/Zn)
B、ε= φ (Ag
(Ag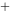 /Ag) -2 φ
/Ag) -2 φ (Zn
(Zn /Zn)
/Zn)
C、ε= φ (Ag
(Ag /Ag) - φ
/Ag) - φ (Zn
(Zn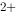 /Zn)
/Zn)
D、ε= φ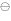 (Zn
(Zn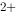 /Zn) - φ
/Zn) - φ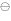 (Ag
(Ag /Ag)
/Ag)
①Ag2S+2e→2Ag+S2-
②1/2Ag2S+e→Ag+1/2S2-
③2Ag+S2-→Ag2S+2e
④Ag+1/2S2-→1/2Ag2S+e
无论采用何种形式,只要电极反应的条件相同,上述各电极反应的电势值均相同。
①Ag2S+2e→2Ag+S2-
②1/2Ag2S+e→Ag+1/2S2-
③2Ag+S2-→Ag2S+2e
④Ag+1/2S2-→1/2Ag2S+e
无论采用何种形式,只要电极反应的条件相同,上述各电极反应的电势值均相同。
A、0.04611V
B、0.05633V
C、0.01337V
D、1.7946V


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题