 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


在探究新制氯水成分及性质的实验中,依据下列方法和现象,不能得出相应结论的是方法 现象 结论()
A.观察氯水颜色 氯水呈黄绿色 氯水中含Cl2
B.向饱和NaHCO3溶液中加入足量氯水 有无色气体产生 氯水中含HClO
C.向红色纸条上滴加氯水 红色纸条褪色 氯水具有漂白性
D.向FeCl2溶液中滴加氯水 溶液变成棕黄色 氯水具有氧化性
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


A.观察氯水颜色 氯水呈黄绿色 氯水中含Cl2
B.向饱和NaHCO3溶液中加入足量氯水 有无色气体产生 氯水中含HClO
C.向红色纸条上滴加氯水 红色纸条褪色 氯水具有漂白性
D.向FeCl2溶液中滴加氯水 溶液变成棕黄色 氯水具有氧化性
 更多“在探究新制氯水成分及性质的实验中,依据下列方法和现象,不能得…”相关的问题
更多“在探究新制氯水成分及性质的实验中,依据下列方法和现象,不能得…”相关的问题
某同学探究同周期元素性质的递变规律,并讨论影响化学反应速率的因素.选用的试剂如下:镁条、铝条、铝粉、钠、新制Na 2 S溶液、新制氯水、0.5mol L -1 盐酸、3mol L -1 盐酸、酚酞试液;其设计的实验方案及部分实验现象如下表: 实验步骤 实验现象 ①将一小块金属钠投入滴有
A.制备Al(OH)3悬浊液:向1mol·L-1aLCl3溶液中加过量的6mol·L-1NaOH溶液
B.提纯含有少量乙酸的乙酸乙酯:向含有少量乙酸的乙酸乙酯中加入过量饱和碳酸钠溶液,振荡后静置分液,并除去有机相的水
C.检验溶液中是否含有Fe3+:取少量待检验溶液,向其中加入少量新制氯水,再滴加KSCN溶液,观察实验现象
D.探究催化剂对H2O2分解速率的影响:在相同条件下,向一支试管中加入2ml5%H2O2和1mlH2O,向另一支试管中加入2mL5%H2O2和1mLFeCl3溶液,观察并比较实验现象
阅读下面文字,回答有关问题:某化学学习小组欲探究铁及其化合物的氧化性和还原性。(1)实验试剂及仪器:氯化亚铁溶液、氯化铁溶液、氯水、KSCN溶液、铁粉、锌片、铜片、稀硫酸、胶头滴管、试管(2)实验记录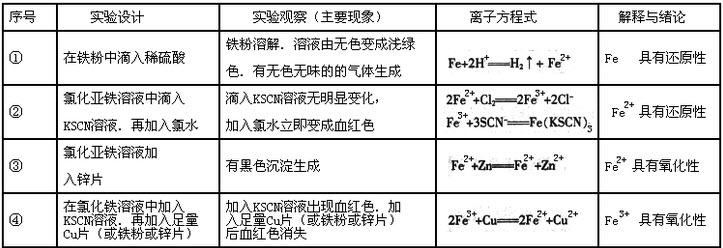
问题:(1)在实验②中,有部分同学在氯化亚铁溶液中滴入KSCN溶液后,就出现了血红色,可能的原因是什么?(2)在配制氯化铁溶液时,由于实验员失误,可能导致溶液中含有少量的Fe2+,如何检验是否有少量Fe的存在?(3)作为教师,在进行实验探究教学时,应注意哪些方面?
下列能够检验出KI中是否含有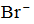 的实验是()
的实验是()
A.加入足量的新制氯水,溶液变色,则有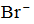
B.加入酸性KMnO4溶液,观察溶液颜色褪去,则有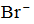
C.加入少量的碘水,再加入CCl4振荡,有机层有色,则有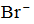
D.加入足量FeCl3溶液,用CCl4萃取后,在无色的水层中加入氯水,溶液呈橙黄色,则含有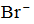
A.金属钠着火燃烧时用水灭火
B.新制氯水保存在棕色试剂瓶中并放置在阴凉处
C.检验铁和水蒸气反应的气体产物时直接点燃
D.直接向容量瓶中加水稀释浓硫酸
(1)实验试剂及仪器:
氯化亚铁溶液、氯化铁溶液、氯水、KSCN溶液、铁粉、锌片、铜片、稀硫酸、胶头滴管、试管
(2)实验记录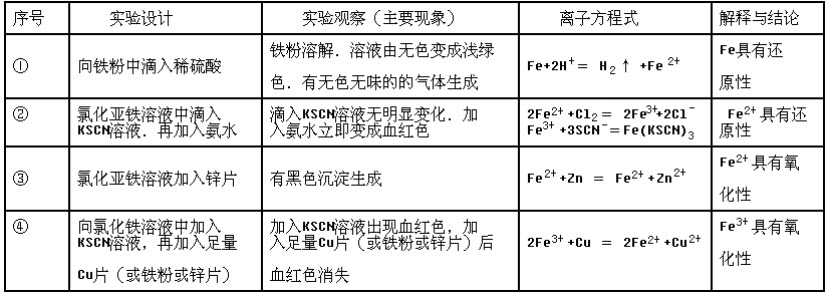
根据上述材料回答下列问题:
(1)在实验②中,有部分同学在氯化亚铁溶液中滴入KSCN溶液后,就出现了血红色,可能的原因是什么?
(2)在配制氯化铁溶液时,由于实验员失误,可能导致溶液中含有少量的Fe,如何检验是否有少量Fe的存在?
(3)作为教师,在进行实验探究教学时,应注意哪些方面?
| (12分)实验室有一瓶密封不严的漂白粉,请利用以下仪器和试剂,完成该漂白粉成分的探究。试管、滴管、带导管的单孔塞、蒸馏水、自来水、1mol/LHCl、品红溶液、新制澄清石灰水。 (1) 提出假设:假设一:该漂白粉未变质,含________________________。 假设二:该漂白粉全部变质,含________________________。 假设三:该漂白粉部分变质,含CaCl2, Ca(ClO)2,CaCO3 (2)进行实验:在答题卡上完成下表(不必检验Ca2+、Cl-)
|
B.Na2SO3溶液中存在
C.依据实验3的现象得出


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题