 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
E Ө(Br2/Br-) = 1.087V,对原电池(-)Pt | H2(10kPa)| H+(1 mol·kg-1 )¦¦ Br–(1 mol·kg-1)| Br2 | Pt(),其电动势为
A.1.087 V
B.1.078 V
C.1.057 V
D.1.117 V
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.1.087 V
B.1.078 V
C.1.057 V
D.1.117 V
 更多“E Ө(Br2/Br-) = 1.087V,对原电池(-)P…”相关的问题
更多“E Ө(Br2/Br-) = 1.087V,对原电池(-)P…”相关的问题
A、3.2´10-2mol·L-1
B、2.5´10-2mol·L-1
C、1.6´10-2mol·L-1
D、4.1´10-2mol·L-1
25℃,101 325 Pa的液态H2O的化学势为 (l),25℃,101 325 Pa的气态H2O的化学势为
(l),25℃,101 325 Pa的气态H2O的化学势为 (g) ,二者的关系是( )
(g) ,二者的关系是( )
A、 (l) >
(l) > (g)
(g)
B、 (l) <
(l) < (g)
(g)
C、 (l) =
(l) = (g)
(g)
D、无法判断
 为0.6158V。
为0.6158V。
(1)(—)Pt|H2(100kPa)|OH-(1.0mol·L-1)||H+(1.0mol·L-1)|H2(100kPa)|Pt ()
(2)(—)Ag|AgI|I-(1.0mol·L-1)||Ag+(1.0mol·L-1)|Ag()
(3)(—)Pt|Cu2+(1.0mol·L-1),Cu+(1.0mol·L-1)||Cu2+(1.0mol· L-1),Cl-(1.0mol·L-1)|CuCl|Pt()
(4)(—)Cu|[Cu(NH3)4]2+(1.0mol·L-1),NH3(1.0mol·L-1)||Cu2+(1.0mol·L-1)|Cu()
有两个电池,电动势分别为E1和E2 H2(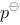 )│KOH(0.1
)│KOH(0.1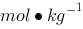 )│O2(
)│O2(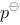 )
)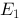 H2(
H2(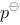 )│H2SO4(0.0l
)│H2SO4(0.0l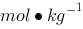 )│O2(
)│O2(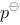 )
)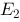 比较其电动势,有 ( )
比较其电动势,有 ( )
A、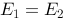
B、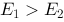
C、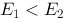
D、不能确定
由两个氢电极H2(100kPa)|H+(0.10mol·dm-3)|Pt和H2(100kPa)|H+(xmol·dm-3)|Pt组成原电池,测得该原电池的电动势为0.016V。若后一电极作为该原电池的正极,求组成该电极的溶液中H+的浓度x的值。
有一电池:
(一)Pt,H2(50.0kPa)| H+(0.50mol/L)|Sn4+(0.70mol/L),Sn2+(0.050mol/L)| Pt(),_______是负极,负极反应为____________________________;_______是正极,正极反应为____________________________;_______为还原剂,_______为氧化剂;电池的总反应为____________________________。
下列电池可用来测定溶液B中Ca2+的浓度。
Hg(l)|Hg2Cl2(s)|KCl(1mol·kg-1)||溶液B|CaC2O4(s)|Hg2C2O4(s)|Hg若用加入NaNO3的方法保持溶液B的离子强度为0.1mol·kg-1,当溶液B中含有0.01mol·kg-1Ca(NO3)2,在298K时测得电池的电动势E1为0.3243V;当溶液B中含Ca2+量不同时,于同样温度下测得E2为0.3111V。


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题