 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用重量法测定某试样中的Fe含量,沉淀形式为Fe(OH)3n·nH2O,称量形式为以Fe2O3,则换算因数为()A.2Fe
用重量法测定某试样中的Fe含量,沉淀形式为Fe(OH)3n·nH2O,称量形式为以Fe2O3,则换算因数为()
A.2FeO/Fe2O3
B.Fe/Fe(OH)3·nH2O
C.Fe2O3/2Fe
D.2Fe/Fe2O3
E.FeO/Fe2O3
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用重量法测定某试样中的Fe含量,沉淀形式为Fe(OH)3n·nH2O,称量形式为以Fe2O3,则换算因数为()
A.2FeO/Fe2O3
B.Fe/Fe(OH)3·nH2O
C.Fe2O3/2Fe
D.2Fe/Fe2O3
E.FeO/Fe2O3
 更多“用重量法测定某试样中的Fe含量,沉淀形式为Fe(OH)3n·…”相关的问题
更多“用重量法测定某试样中的Fe含量,沉淀形式为Fe(OH)3n·…”相关的问题
用重量法测定某试样中的Fe,沉淀形式为Fe(OH)3*nH2O,称量形式为Fe2O3,换算因数应为()。
A.Fe/Fe(OH)3*nH2O
B.Fe/Fe2O3
C.2Fe/Fe2O3
D.Fe2O3/Fe
E.Fe2O3/2Fe
用重量法测定某试样中的FeO,沉淀形式为Fe(OH)3.nH20,称量形式为Fe203,则换算因素为
A.Fe(OH)3.nH20/Fe203
B.2Fe(OH)3.nH2/Fe203
C.FeO/Fe203
D.2FeO/Fe203
E.Fe203/2FeO
锰及其他金属元素,称取127.3mg试样溶解在酸中并加入适当掩蔽剂,以防止其他金属离子的干扰。铁和锰分别以Fe(C9H6NO)3(相对分子质量:488.28) 和Mn(C9H6NO)2(相对分子质量:343.23) 的形式沉淀,共得到沉淀867.8mg,同时用去8-羟基喹啉5.276mmol.试分别计算铁和锰的含量。
用重量法测定试样中的镁的含量,MgNH4PO4为沉淀形式,Mg2P2O7为称量形式。测定叫wMg时的换算因子是______,测定wMgO时的换算因子是______。
用重量法测定试样中镁的含量,MgNH4PO4为沉淀形式,Mg2P2O7为称量形式。测定wMg时的换算因子是______,测定训wMgO时的换算因子是______。
某试样中约含50%的BaO,用BaSO4重量法测定其准确含量时,其中的Fe3+将共沉淀,若Fe3+共沉淀的量为溶液中。Fe3+含量的5%,那么要使Fe3+共沉淀引起的误差不大于0.1%,试样中Fe的含量应少于多少?[M(BaSO4)=233.39g·mol-1,M(Fe2O3)=159.69g·mol-1,M(BaO)=153.33g·mol-1,M(Fe)=55.847g·mol-1]
称取试样0.5000g,用重量法测定镁的含量,MgNH4PO4为形式沉淀,Mg2P2O7为称量形式。测得Mg2P2O70.4200g,求w(Mg)与w(MgO)。
某试样中含MgO约30%,用重量法测定其含量时,Fe3+产生共沉淀,设试液中的Fe3+有1%进入沉淀。若要求测定结果的相对误差小于0.1%,求试样中Fe2O3允许的最高质量分数为多少?
称取试样0.5000g,用重量法测定镁的含量,MgNH4PO4为沉淀形式,Mg2P2O7为称量形式。测得Mg2P2O70.4200g,求质量分数ω(Mg)与ω(MgO)。[M(Mg)=24.30g·mol-1]M(Mg2P2O7)=222.6g·mol-1,M(MgO)=40.32g·mol-1]
用BaSO4重量法测定Ba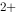 含量,若结果偏低,可能是由于-------------------------()
含量,若结果偏低,可能是由于-------------------------()
A、沉淀中含有Fe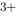 等杂质
等杂质
B、沉淀中包藏了BaCl2
C、沉淀剂H2SO4在灼烧时挥发
D、沉淀灼烧的时间不足


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题